一定温度下,在三个体积约为1.0L的恒容密闭容器中发生反应:
2CH3OH(g) CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
| 容器 编号 |
温度(℃) |
起始物质的量(mol) |
平衡物质的量(mol) |
|
| CH3OH(g) |
CH3OCH3(g) |
H2O(g) |
||
| I |
387 |
0.20 |
0.080 |
0.080 |
| Ⅱ |
387 |
0.40 |
|
|
| Ⅲ |
207 |
0.20 |
0.090 |
0.090 |
下列说法正确的是
A.该反应的正方应为放热反应
B.达到平衡时,容器I中的CH3OH体积分数比容器Ⅱ中的小
C.容器I中反应达到平衡所需时间比容器Ⅲ中的长
D.若起始时向容器I中充入CH3OH 0.1mol、CH3OCH3 0.15mol和H2O 0.10mol,则反应将向正反应方向进行
Al、Fe、Cu都是重要的金属元素。下列说法正确的是
| A.三者对应的氧化物均为碱性氧化物 |
| B.三者的单质放置在空气中只生成氧化物 |
| C.制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法 |
| D.电解AlCl3、FeCl3、CuCl2的混合溶液在阴极上依次析出Cu、Fe、Al |
用NA表示阿伏加德罗常数,下列说法正确的是
A.0.l mol的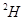 分子中的中子数是2 分子中的中子数是2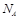 |
B.标准状况下,一定量的铜与硝酸反应后生成22.4 LNO、NO2、N2O4的混合气体,则被还原的硝酸的分子数大于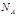 |
C.100mL 1 mol /LNa[Al(OH)4]溶液中含有0.1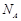 个[Al(OH)4]- 个[Al(OH)4]- |
| D.1 mol羟基和1mol氢氧根离子中的电子数和质子数均相等 |
下列说法中,正确的是
| A.人造纤维、合成纤维和光导纤维都是有机高分子化合物 |
| B.钢铁制品和铜制品既能发生吸氧腐蚀又能发生析氢腐蚀 |
| C.明矾用于净水既与盐类的水解有关,又与胶体的眭质有关 |
| D.棉花、羊毛及台成纤维完全燃烧都只生成二氧化碳和水 |
某溶液中可能含有 。某兴趣小组为确定该溶液的组成,进行了下列实验:取样,滴加足量氯水,有气泡产生,溶液呈橙色;向橙色溶液中加BaCl2溶液或淀粉均无明显变化。下列说法正确的是
。某兴趣小组为确定该溶液的组成,进行了下列实验:取样,滴加足量氯水,有气泡产生,溶液呈橙色;向橙色溶液中加BaCl2溶液或淀粉均无明显变化。下列说法正确的是
| A.溶液中一定存在Na+、I-、CO32- |
| B.溶液中一定不存在的只有I-、SO32- |
| C.只需再进行一个实验,就可完全确定溶液的组成 |
| D.溶液中一定存在Br-、CO32-,至少存在Na+、NH4+中的一种 |
特斯拉全电动汽车使用的是钴酸锂电池,其工作原理如右图,A 极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料,隔膜只允许 Li+通过,电池反应式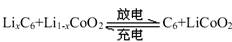 。下列说法不正确的是
。下列说法不正确的是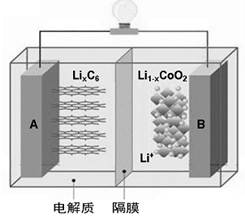
| A.放电时电子从A极通过导线流向B极 |
| B.放电时A是负极,电极反应式为:LixC6-xe-=C6+xLi+ |
| C.充电时Li+从左边流向右边 |
D.充电时B作阳极,电极反应式为: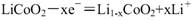 |