短周期主族元素A、B、C、D、E的原子序数依次递增,A、B两元素相邻,B、C、E原子的最外层电子数之和为13,E原子最外层电子数是B原子内层电子数的3倍或者C原子最外层电子数的3倍,B、D原子最外层电子数之和等于C、E原子最外层电子数之和。下列说法正确的是
A.元素B和E的氧化物对应的水化物均为强酸
B.工业上常用电解元素C、D的氯化物来制取它们的单质
C.元素C、D、E的最高价氧化物对应的水化物之间均可相互反应
D.C的单质能与A的氧化物发生置换反应
一定温度下,硫酸铜受热分解生成CuO、SO2、SO3和O2。已知:SO2、SO3都能被碱石灰和氢氧化钠溶液吸收。利用图所示装置加热硫酸铜粉末直至完全分解。硫酸铜粉末质量为10.0 g,完全分解后,各装置的质量变化关系如下表所示。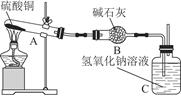
| 装置 |
A(试管+粉末) |
B |
C |
| 反应前 |
42.0 g |
75.0 g |
140.0 g |
| 反应后 |
37.0 g |
79.5 g |
140.0 g |
请通过计算,推断出该实验条件下硫酸铜分解的化学方程式是( )
A.4CuSO4 4CuO+2SO3↑+2SO2↑+O2↑
4CuO+2SO3↑+2SO2↑+O2↑
B. 3CuSO4 3CuO+SO3↑+2SO2↑+O2↑
3CuO+SO3↑+2SO2↑+O2↑
C.5CuSO4 5CuO+SO3↑+4SO2↑+2O2↑
5CuO+SO3↑+4SO2↑+2O2↑
D.6CuSO4 6CuO+4SO3↑+2SO2↑+O2↑
6CuO+4SO3↑+2SO2↑+O2↑
下列根据实验操作和现象所得出的结论正确的是( )
| 选项 |
实验操作 |
实验现象 |
结 论 |
| A |
将少量Fe(NO3)2试样加水溶解,滴加稀H2SO4酸化,再滴加KSCN溶液 |
溶液变成红色 |
Fe(NO3)2试样已变质 |
| B |
将少量某无色气体通入澄清石灰水 |
出现白色沉淀 |
该气体一定是CO2 |
| C |
分别测定常温下0.1 mol·L-1 Na2SiO3溶液和Na2CO3溶液的pH |
pH:Na2SiO3> Na2CO3 |
非金属性:Si>C |
| D |
向浓度均为0.1 mol·L-1 NaCl和NaI混合溶液中,滴加少量AgNO3溶液 |
出现黄色沉淀 |
Ksp(AgCl)>Ksp(AgI) |
选用实验装置完成对应的实验,能达到目的的是( )
下列有关实验原理或实验操作正确的是( )
| A.用(a)装置制备并收集少量NO2气体 |
| B.通过(b)装置实现化学反应:2Cu+O2+4H+=2Cu2++2H2O |
| C.装置(c)可用于定量测定H2O2的分解速率 |
| D.装置(d)可用于实验室制取乙酸乙酯 |
下列实验设计能够成功的是( )
A.检验亚硫酸钠试样是否变质:试样 白色沉淀 白色沉淀 沉淀不溶解―→说明试样已变质 沉淀不溶解―→说明试样已变质 |
B.除去粗盐中含有的硫酸钙杂质粗盐   精盐 精盐 |
C.检验某溶液中是否含有Fe2+试样 溶液颜色无变化 溶液颜色无变化 溶液变红色―→溶液中含有Fe2+ 溶液变红色―→溶液中含有Fe2+ |
D.证明酸性条件H2O2的氧化性比I2强:NaI溶液 溶液变蓝色―→氧化性:H2O2>I2 溶液变蓝色―→氧化性:H2O2>I2 |