【改编】下列有关判断正确的是
| A.0.1mol/LNa2CO3溶液:c(Na+)= 2c(H2CO3)+2 c(HCO3-)+ c(CO32‾) |
| B.能使酚酞溶液呈红色的溶液:Na+、Ba2+、I-、NO3-可以大量共存 |
| C.任何条件下,pH=1的硫酸溶液中:c(H+)=0.1mol/L |
| D.将0.2 mol·L-1的HCN溶液和0.1 mol·L-1的NaOH溶液等体积混合,溶液显碱性,则c(HCN)=c(CN-)= c(Na+) |
下列物质性质与应用及其对应关系均正确的是
| 选项 |
性质 |
应用 |
| A |
碳酸氢钠可与烧碱反应 |
可用碳酸氢钠作糕点膨松剂 |
| B |
AgCl难溶于稀硝酸 |
可用稀硝酸和AgNO3溶液检测Cl一 |
| C |
浓硫酸具有强氧化性,而稀硫酸的氧化性较弱 |
可用浓硫酸替代稀硫酸与锌反应快速制氢气 |
| D |
碳单质性质稳定 |
可在纯铁中加入少量炭增强抗腐蚀性 |
下列物质转化无法实现的是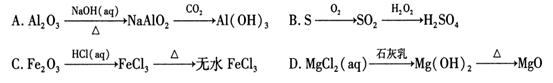
下列溶液中,相关微粒的浓度关系正确的是
| A.MgSO4溶液:c(Mg2+)+c(H+)=" c" (SO42一)+c(OH一) |
| B.将0.2mol·L-1CH3 COOH溶液与0.1mo1·L-1NaOH溶液等体积混合:c(CH3 COO一)+ c(CH3COOH)=2c(Na+) |
| C.将pH=2的盐酸与0.01 mo1·L-1氨水等体积混合:c(NH4+)=" c" (Cl一) |
| D.由AgCl和AgI固体混合物与水形成的悬浊液:c(Ag+)>c(Cl一) =" c" (I一) |
下列实验结论正确的是
| A.向某溶液中加入稀盐酸,产生的气体通人澄清石灰水,石灰水变浑浊,该溶液一定是碳酸盐溶液 |
| B.用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定不含K+ |
| C.将某气体通人溴水中,溴水颜色褪去,该气体一定是SO2 |
| D.向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含Fe2+ |
将反应Cu(s)+2Ag+(aq)=Cu2+(aq)+2Ag(s)设计成如图所示的原电池,下列叙述正确的是
| A.KNO3盐桥中的K+移向Cu(NO3)2溶液 |
| B.Ag作负极,Cu作正极 |
| C.工作一段时间后,Cu(NO3)2溶液中c(Cu2+)增大 |
| D.取出盐桥后,电流计的指针依然发生偏转 |