选做【化学——选修2:化学与技术】海洋是一个丰富的资源宝库,通过海水的综合利用可获得许多物质供人类使用。
(1)海水中盐的开发利用:
①海水制盐目前以盐田法为主,建盐田必须选在远离江河入海口,多风少雨,潮汐落差大且又平坦空旷的海滩。所建盐田分为贮水池、蒸发池和 池。
②目前工业上采用比较先进的离子交换膜电解槽法进行氯碱工业生产,在电解槽中阳离子交换膜只允许阳离子通过,阻止阴离子和气体通过,请说明氯碱生产中阳离子交换膜的作用 (写一点即可)。
(2)电渗析法是近年来发展起来的一种较好的海水淡化技术,其原理如图所示。其中具有选择性的阴离子交换膜和阳离子交换膜相间排列。请回答下面的问题:
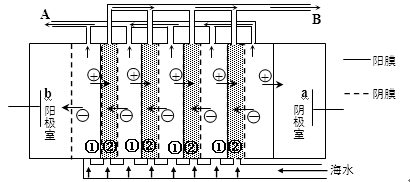
①海水不能直接通入到阴极室中,理由是 。
②A口排出的是 (填“淡水”或“浓水”)。
(3)用苦卤(含Na+、K+、Mg2+、Cl-、Br-等离子)可提取溴,其生产流程如下:
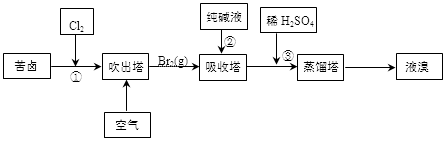
①若吸收塔中的溶液含BrO3-,则吸收塔中反应的离子方程式为 。
②通过①氯化已获得含Br2的溶液,为何还需经过吹出、吸收、酸化来重新获得含Br2的溶液 。
③向蒸馏塔中通入水蒸气加热,控制温度在90℃左右进行蒸馏的原因是 。
组成生命细胞的11种常量元素(约占人体总质量的99.97%),全部位于周期表的前20号。其中组成人体蛋白质、脂肪、碳水化合物和核酸的主要有6种元素。
(1)这六种元素中除H、C、O、P、S外,应该还有____(写元素符号),它的基态原子核外电子排布式是,其第一电离能比O的________(填“大”或“小”);与它同周期,且单质熔点最高的元素在周期表中的位置。
(2)CO2是一种温室气体,它的电子式为,将其转变其他化工原料,必须 破坏的化学键属于(填“极性”或“非极性”)键。
破坏的化学键属于(填“极性”或“非极性”)键。
(3)元素周期表中元素的性质存在递变规律,下列关系正确的是____(填序号)。
a.离子半径:S2-> Na+>O2->H+ b.与水反应的剧烈程度:K>Na>Mg>Ca
c.熔点:CO2>SiO2>Na2O>SO3 d.还原性:PH3>H2S>HCl>HF
(4)下表为部分非金属元素与氢形成共价键的键长与键能数据:
根据表中数据,归纳共价键键能与键长的关系
。
NaBH4(硼氢化钠)是典型的离子化合物,在有机反应中可将醛、酮变为醇。
(1)硼氢化钠与水反应的离子方程式是BH4—+2H2O=BO2—+4H2↑,该反应中氧化剂是____________,生成1mol H2时转移电子的数目是_____________________。
(2)已知HBO2是弱酸,溶液的酸性对硼氢化钠与水的反应速率有影响,酸性越强,其反应速率越____,这是因为。
(3)硼氢化钠能把许多金属离子还原为金属单质,为抑制它与水的反应,反应在________ (填“酸性”“中性”或“碱性”)条件下进行,试完成并配平金离子(Au3+)被硼氢化钠还原的离子方程式:____Au3++____BH4—+__________=____Au↓+____BO2— +__________。
在下列各变化中,反应①为常温下的反应,A 、C、D均含氯元素,且A中氯元素的化合价介于C与D之间,E常温下为无色无味的液体,F为淡黄色粉末,G为常见的无色气体。
、C、D均含氯元素,且A中氯元素的化合价介于C与D之间,E常温下为无色无味的液体,F为淡黄色粉末,G为常见的无色气体。
回答下列问题:
(1)A、G的化学式分别为___ ___、______。
(2)A和E反应的离子方程式为______。
(3)写出反应①的化学方程式______________________________。
(4 )在反应②中,每生成2.24 L气体G(标准状况)时,消耗F ____g。
)在反应②中,每生成2.24 L气体G(标准状况)时,消耗F ____g。
有一固体粉末,其中可能含有Na2CO3、NaCl、Na2SO4、CuCl2、Ba(NO3)2、K2CO3、K2SO4中的一种或几种,现按下列步骤进行实验。
(1)将该粉末溶于水得无色溶液和白色沉淀。
(2)在滤出的沉淀中加入稀硝酸,有部分沉淀溶解,同时产生无色气体。
(3)取滤液做焰色反应,火焰呈黄色,透过蓝色的钴玻璃观察,未见紫色火焰。
由上述现象推断:
该混合物中一定含有、、;一定不含有、、;可能含有。
用20.0g烧碱配制成500mL溶液,其物质的量浓度为mol·L-1;从中取出10mL,其物质的量浓度为mol·L-1。若将这10mL溶液用水稀释到100mL,所得溶液中溶质的物质的量浓度为mol·L-1。