某化学活动小组需要用溶质质量分数为19.6%的稀硫酸和锌粒反应来制取氢气,但实验室现有的是溶质质量分数为98%的浓硫酸。试计算:
(1)将50g浓硫酸配制成所需的稀硫酸,需要水的质量为多少?
(2)取上述配制好的稀硫酸100g与20g铜锌合金恰好完全反应。求参加反应的锌的质量分数和反应生成的氢气质量?(反应的化学方程式为Zn +H2SO4=ZnSO4 + H2↑)
加热氯酸钾和二氧化锰固体混合物制取氧气时,反应时间和剩余固体质量如图.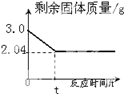
(1)根据质量守恒定律,该反应产生的氧气质量为g.
(2)求原固体混合物中氯酸钾的质量是多少?
某补钙药品说明书的部分信息如图所示。
现取4 片钙片放入100g稀盐酸中,有效成分完全反应(其他它成分不与稀盐酸反应),反应过程中质量的变化如下。
| 反应前 |
烧杯 |
50g |
| 4片钙片 |
8g |
|
| 稀盐酸 |
100g |
|
| 完全反应后 |
烧杯+剩余固体+液体的总质量 |
155.36g |
(1)反应生成二氧化碳的质量是g。
(2)通过计算回答,该补钙药品说明书中碳酸钙的含量与实际是否相符。
甲基硅酸钠(化学式为CH5SiO3Na)是一种新型建筑防水材料。
(1)甲基硅酸钠由 种元素组成,其相对分子质量是。
(2)甲基硅酸钠中各元素的质量比是C:H:Si:O:Na=。
(3)甲基硅酸钠中钠元素的质量分数是。
某铁合金5.8g,与足量的稀硫酸充分反应,得到0.2g的氢气。请计算:
(1)该合金中铁的质量是多少克?
(2)该合金是生铁还是钢?(已知:生铁的含碳量是2%—4%,钢的含碳量是0.03%—2%)
尿素[CO(NH2)2]溶液可用作柴油汽车尾气处理液。用尿素溶液处理柴油汽车尾气(含NO)时的化学方程式如下(反应条件略去):
2CO(NH2)2 + 4NO + O2 = 2CO2+ 4N2 + 4H2O。
用含24千克的尿素配成的溶液处理柴油汽车尾气(含NO),可吸收NO的质量是多少?