已知:常温下浓度为0.1 mol·L-1的下列溶液的pH如表:
| 溶质 |
NaF |
NaClO |
Na2CO3 |
| pH |
7.5 |
9.7 |
11.6 |
下列有关说法正确的是
A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:H2CO3<HClO<HF
B.若将CO2通入0.1 mol·L-1Na2CO3溶液中至溶液中性,则溶液中2c(CO32ˉ)+ c(HCO3ˉ)=" 0.1" mol·L-1
C.根据上表, 水解方程式ClOˉ+ H2O HClO + OHˉ的平衡常数K≈10ˉ7.6
HClO + OHˉ的平衡常数K≈10ˉ7.6
D.向上述NaClO 溶液中通HF气体至恰好完全反应时:
c(Na+)>c(Fˉ)>c(H+)>c(HClO)>c(OHˉ)
有关下列图像的分析错误的是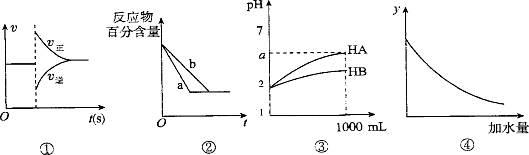
A.图①可表示对平衡N2(g)+3H2(g)  2NH3(g)加压、同时移除部分NH3时的速率变化。
2NH3(g)加压、同时移除部分NH3时的速率变化。
B.图②中a、b曲线只可表示反应H2(g)十I2(g)  2HI(g)在有催化剂和无催化剂存在下建立平衡的过程。
2HI(g)在有催化剂和无催化剂存在下建立平衡的过程。
C.图③表示室温下将各1 ml pH=2的HA、HB两种酸溶液加水稀释的情况。若2<a<5,则两酸都为弱酸
D.图④中的y可表示将0.1 mol/l稀醋酸加水稀释时溶液导电能力的变化情况
恒温、恒压下,将1 mol O2和2 mol SO2气体充入一个体积可变的容器中(状态Ⅰ) ,发生反应:2SO2(g)+O2(g) 2SO3(g),状态Ⅱ时达平衡,则O2得转化率为:
2SO3(g),状态Ⅱ时达平衡,则O2得转化率为:
| A.60% | B.40% | C.80% | D.90% |
下列有关水电离情况的说法正确的是
| A.25℃,pH=12的烧碱溶液与纯碱溶液,水的电离程度相同 |
| B.其它条件不变,稀释醋酸钠溶液,水的电离程度增大 |
| C.其它条件不变,稀释氢氧化钠溶液,水的电离程度减小 |
| D.其它条件不变,温度升高,水的电离程度增大,Kw增大 |
下列叙述正确的是
A.稀硝酸、稀硫酸均能将木炭氧化成二氧化碳
B.Na2O2与水反应,红热的Fe与水蒸气反应均能生成碱
C.Li、C、P分别在足量氧气中燃烧均生成一种相应氧化物
D.NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体
下列离子方程式书写正确的是
A.用Pt电极电解少量的MgCl2溶液:2H2O+2Cl- H2↑+Cl2↑+2OH- H2↑+Cl2↑+2OH- |
| B.H218O中投入Na2O2固体:2H218O+2O22-=4OH-+18O2↑ |
| C.Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-= CaCO3↓+H2O |
| D.FeSO4溶液中加H2O2溶液:Fe2++2H2O2+4H+= Fe3++4H2O |