固体粉末X中可能含有Cu、FeO、Fe2O3、NaHCO3、Na2CO3、Na2S2O3、NaAlO2中的若干种。某化学兴趣小组为确定该固体粉末的成分,现取X进行连续实验,实验过程及现象如下:
已知:HCO3-+AlO2-+H2O=Al(OH)3↓+CO32-
下列说法正确的是
| A.气体乙和气体丙都为纯净物 |
| B.固体粉末X中一定含有FeO、Na2S2O3、NaAlO2,可能含有NaHCO3、Na2CO3 |
| C.溶液丁中的阳离子一定只含H+、Fe2+ |
| D.溶液甲中一定含有AlO2-,可能含有CO32- |
某实验人员做了下列实验:将一定量1.00mol/L CuSO4溶液和2.00mol/LNaOH溶液混合,得到一种浅绿色沉淀X。将0.454g X隔绝空气在1000℃以上强热,得到一种红色固体Y,质量为0.288g。Y溶于稀硫酸得到另一种红色固体0.128g(已知铜的化合价有+1和+2价)。
(1)该实验人员认为沉淀X可能含有SO42-。请设计一个简单实验确定这一判断。
(2)Y与稀硫酸反应的离子方程式为:。
(3)通过计算确定X的组成?
(4)混合时CuSO4和NaOH溶液的体积比为;写出X→Y的反应方程式::
。
过氧化氢是一种无色透明的无毒液体,是重要无机化工产品。试探究下列问题
(1)过氧化氢最适合贴上的一个标签是 。
|

 (NH4)2S2O8 + H2↑,
(NH4)2S2O8 + H2↑,


竖炉冶铁工艺流程如图,使天然气产生部分氧化,并在特殊的燃烧器中使氧气和天然气燃烧CH4(g)+2O2(g)=CO2(g)+2H2O(g),催化反应室发生的反应为:CH4(g)+H2O(g)  CO(g)+3H2(g);△H1=+216kJ/mol;CH4(g)+ CO2(g)
CO(g)+3H2(g);△H1=+216kJ/mol;CH4(g)+ CO2(g) 2CO(g) + 2H2(g); △H2=+260kJ/mol(不考虑其他平衡的存在),下列说法正确的是
2CO(g) + 2H2(g); △H2=+260kJ/mol(不考虑其他平衡的存在),下列说法正确的是
| A.增大催化反应室的压强,甲烷的转化率减小 |
| B.催化室需维持在550~750℃,目的仅是提高CH4转化的速率 |
| C.设置燃烧室的主要目的是产生CO2和水蒸气作原料气与甲烷反应 |
| D.若催化反应室中,达到平衡时,容器中n(CH4)=amol,n(CO)=bmol |
n(H2)=cmol,则通入催化反应室的CH4的物质的量为a+(b+c)/4
硒被称为主宰生命的元素之一,人们开发了一种含有钙铁锌硒(Ca、Fe、Zn、Se)的保健品。下列说法正确的是
| A.四种元素均处于第4周期,且均是主族元素 |
| B.H2Se比H2O热稳定性好 |
| C.单质钙能将FeSO4溶液中铁置换出来 |
D.与保健品中苏氨酸互为同分异构体的硝酸酯(RONO2)有四种 |
下列有关说法正确的是
| A.SO2(g)+H2O(g)→H2SO3(l),该过程熵值增大 |
| B.SO2(g)→S(s)+O2(g)△H>0,△S<0该反应能自发进行 |
| C.SO2(g)+2H2S(g)=3S(s)+2H2O(l) ,常温常压下一定能自发进行 |
D.某温度下SO2(g)+1/2O2(g)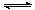 SO3(g),K1=20, SO3(g),K1=20, |
则相同温度下2SO3(g) 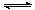 2SO2(g)+O2(g)的平衡常数为1/400
2SO2(g)+O2(g)的平衡常数为1/400