铁及其化合物在日常生活中有广泛应用。
(1)写出Fe(OH)2转化为Fe(OH)3的化学方程式 。
(2)绿矾(FeSO4·7H2O)是补血剂的原料,易变质。检验绿矾是否变质的试剂是
设计实验检验绿矾是否完全变质
(3)利用绿矾制备还原铁粉的工业流程如下:
①干燥过程主要是为了脱去游离水和结晶水,过程中会有少量FeCO3·nH2O在空气中被氧化为FeOOH,该反应的化学方程式为
②取干燥后的FeCO3样品12.49g ,焙烧,最终得到还原铁粉6.16g,计算样品中杂质FeOOH的质量
(4)以羰基化合物为载体运用化学平衡移动原理分离、提纯某纳米级活性铁粉(含有一些不反应的杂质),反应装置如下图。
Fe(s)+5CO(g)  Fe(CO)5(g) ΔH<0
Fe(CO)5(g) ΔH<0
T1 T2(填“>”、“<”或“=”),判断理由是
某学生利用锌与稀硫酸反应产生的氢气的体积,粗略测定锌的摩尔质量(设Wg锌片全部反应,产生气体的体积折算成标准状况时不超过50mL)。实验装置如下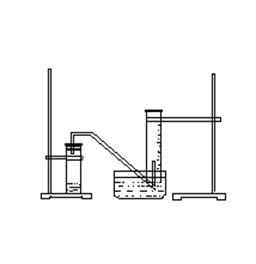
请回答:(1)进行此实验时,必须保证气密性良好,如何检验此装置的气密性?
______________________________________________________________________________________________________________________________________________
(2)以下是测量收集到气体体积必须包含的几个步骤:a.调整量筒内外液面高度使之相同;b.使试管和量筒内的气体都冷却至室温;c.读取量筒内气体的体积。这三个操作步骤的正确顺序是(填写代号) _____________________。
测量收集到气体体积时,如何使量筒内外液面的高度相同?
_____________________________________________________________________
进行该操作的目的是___________________________________________
如果实验中得到的氢气体积是VmL(已折算成标准状况),水蒸气的影响忽略不计
锌的摩尔质量的计算式为(含W、V,不必化简):M(Zn)= _______________________
甲乙两位同学分别用不同的方法配制100mL 3.6mol/L的稀硫酸。
(1)若采用18mol/L的浓硫酸配制溶液,需要用到浓硫酸的体积为_________ 。
(2)甲学生:量取浓硫酸,小心地倒入盛有少量水的烧杯中,搅拌均匀,待冷却至室温后转移到100 mL 容量瓶中,用少量的水将烧杯等仪器洗涤2~3次,每次洗涤液也转移到容量瓶中,然后小心地向容量瓶加入水至刻度线定容,塞好瓶塞,反复上下颠倒摇匀。
①将溶液转移到容量瓶中的正确操作是
______________________________________________________________________________。
②洗涤操作中,将洗涤烧杯后的洗液也注入容量瓶,其目的是
______________________________________________________________________。
③定容的正确操作是
______________________________________________________________________。
④用胶头滴管往容量瓶中加水时,不小心液面超过了刻度,处理的方法是________(填序号)。
| A.吸出多余液体,使凹液面与刻度线相切 |
| B.小心加热容量瓶,经蒸发后,使凹液面与刻度线相切 |
| C.经计算加入一定量的浓盐酸 |
| D.重新配制 |
(3)乙学生:用100 mL 量筒量取浓硫酸,并向其中小心地加入少量水,搅拌均匀,待冷却至室温后,再加入水至100 mL 刻度线,再搅拌均匀。你认为此法是否正确?若不正确,指出其中错误之处
____________________________________________________________________________
用质量分数为98%、密度为1.84g/cm3的浓硫酸配制100mL1.84mol/L的稀硫酸,若实验仪器有:
| A.100mL量筒 | B.托盘天平 |
| C.玻璃棒 | D.50mL容量瓶 |
E.10mL量筒 F.胶头滴管
G.50mL烧杯 H.100mL容量瓶
实验时应选用仪器的先后顺序是(填入编号):。
“化学多米诺实验”是利用化学反应中气体产生的压力,使多个化学反应依次发生。下图所示就是一个“化学多米诺实验”,其中A~F装置中分别盛放的物质为:
| A.稀硫酸; | B.锌粒; |
| C.某溶液; | D.CaCO3固体; |
E、滴有紫色石蕊试液的蒸馏水;F、足量的澄清石灰水
请回答下列问题:
(1)反应开始后,若E中出现红色,F中有白色沉淀生成,则C中的物质可能是(填名称)。
(2)写出下列装置中发生反应的离子方程式及反应类型:
装置D中:反应类型:
装置F中:反应类型:
(3)上图所示的B~F装置中,发生了氧化还原反应的是(填装置编号)。
某校的探究小组同学想研究氧化铜能否在氯酸钾的受热分解反应中起催化剂的作用,设计了以下的对比实验和操作步骤:
①任取两份氯酸钾,分别放入两支试管,在其中一份中加入经精确称量的n g氧化铜粉末。
②将两份氯酸钾同时在相同的条件下加热,将放出的气体通入水中,观察放出气体的快慢。
③停止加热、冷却,将原先混有氧化铜的反应后的混合物加水溶解,小心过滤,将滤出固体物质洗涤并干燥。
④观察滤出固体物质的状态、颜色。
⑤将滤出固体物质和炭粉混合,在密闭容器中加热,并将反应产生的气体通入澄清石灰水中,并观察实验现象。
(1)从以上有关实验步骤的叙述中可发现操作方案还存在一些缺陷,请指出并加以改进:
______________________________________________________________________、
______________________________________________________________________。
(2)有人换用另一种方法来代替上述第⑤操作,请从下图中选择仪器中连接成一套实验装置,这套实验装置的连接顺序是_______接______、________接______、________接________接_______(气流的方向从左往右)。