随着经济的不断发展,人们对环境问题也越来越关注。
(1)室内空气污染问题得到越来越多的关注,下列物质中也属于室内挥发性有机污染物的是_____。(填字母)
a.苯 b.甲烷 c.醋酸 d.乙烯
(2)下列措施中,有利于降低室内污染物浓度的是__________。(填字母)
a.勤开窗通风
b.日常生活中利用天然气替代煤作燃料
c.使用“绿色环保”装饰材料
d.室内放一些活性碳
(3)“温室效应”是全球关注的环境问题之一。CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决温室效应的有效途径。将CO2转化成有机物可有效实现碳循环。CO2转化成有机物的例子很多,如:
a.6CO2 + 6H2O C6H12O6+6O2
C6H12O6+6O2
b.CO2 + 3H2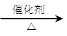 CH3OH +H2O
CH3OH +H2O
c.CO2 + CH4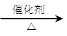 CH3COOH
CH3COOH
d.2CO2 + 6H2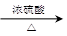 CH2==CH2 + 4H2O
CH2==CH2 + 4H2O
以上反应中,最节能的是 ,原子利用率(原子利用率=期望产物的总质量与生成物的总质量之比)最高的是 。
(4)氟氯代烷(商品名氟利昂)曾被广泛用作制冷剂、灭火剂、溶剂等,因氯、溴的氟代烷对____产生破坏作用而被禁止、限制使用。
(5)“汽车尾气污染”已倍受世人关注。以辛烷(C8H18)代表汽油的成分,要使辛烷正好完全燃烧,则辛烷气与空气(空气中O2占1/5体积)的体积比(相同条件下)为 (保留三位小数)。
通过实验测定反应速率的方法有多种,如比较锌粒与不同浓度硫酸反应时的速率,可通过测定收集等体积H2需要的____________来实现;在KMnO4与H2C2O4反应中,可通过测定____________________________来测定该反应的速率;在Na2S2O3和H2SO4反应中,该反应的速率可通过__________________________来测定。写出KMnO4与H2C2O4反应的离子方程式:。
在下列事实中,什么因素影响了化学反应速率:
(1)集气瓶中H2和Cl2的混合气体,在瓶外点燃镁条时发生爆炸:_____________________。
(2)熔化的KClO3放出气泡很慢,撒入少量MnO2很快产生气体:_____________________。
(3)同浓度.同体积的盐酸中分别放入同样大小的锌粒和镁条,产生气体有快有慢:______________________________。
(4)夏天的食品易霉变,而冬天不易发生该现象:________________________。
由铁矿石生产金属铁有两种可能的途径:
①Fe2O3(s)+3∕2C(s)="=2Fe(s)+" 3∕2CO2(g)
△H=231.93kJ·mol-1△S=276.32J·mol-1·K-1
②Fe2O3(s)+3H2(g)==2Fe(s)+3H2O(g)
△H=96.71kJ·mol-1△S=138.79J·mol-1·K-1
(1)试判断这两个反应在高温还是低温下自发进行。
(2)上述反应中的(填序号)可以在较低温度下进行。
已知反应N2O4(g)==2NO2(g)△H=57.24kJ·mol-1△S=176J·mol-1·K-1则在298.15K时该反应自发向进行(填“左”或“右”),在500K时反应自发向进行。
12分)判断下列过程的熵变的正负(填“>0”或“<0”)
(1) 溶解少量蔗糖于水中, △S__________;
(2) 纯碳和氧气反应生成 CO(g), △S__________;
(3) 液态水蒸发变成水蒸气, △S____________;
(4) CaCO3(s)加热分解生成CaO(s)和CO2(g),△S____________。