Ⅰ.现有CH4、C2H4、苯三种有机化合物:
(1)等质量的以上三种物质完全燃烧时耗去O2的量最多的是_______。
(2)等物质的量以上三种物质完全燃烧时耗去O2的量最多的是________。
(3)等质量的以上三种物质完全燃烧时生成CO2的量最多的是________。
Ⅱ.按要求书写:
(1)羟基的电子式 ;
(2)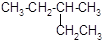 的系统命名为 。
的系统命名为 。
(3)相对分子质量为72且沸点最低的烷烃的结构简式 ;
(4)某芳香烃的相对分子质量为102,若该分子内所有原子均在同一平面内,则其结构简式为 。
如图所示的A、B、C、D、E五种物质的相互转化关系,按如下要求填写相应的物质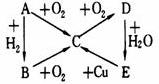
当A是气体单质时,B是______,C是_____,E是______。
浓硫酸在下列用途和现象中所表现的性质是(用编号填写)
| A.沸点高、难挥发 | B.酸性 | C.吸水性 | D.脱水性 E、强氧化性 |
| 用途或现象 |
体现浓硫酸的性质 |
| (1)浓硫酸使蓝矾变成白色 |
|
| (2)浓硫酸使木条变黑 |
|
| (3)浓硫酸制HCl |
|
| (4)浓硫酸与铜片共热 |
|
| (5)浓硫酸与木炭共热产生气体 |
写出有关的元素符号或名称
(1)某元素最外层电子数是次外层电子数的2倍,该元素符号是。
(2)某元素K层与M层电子数相同,该元素名称是。
写出下列反应化学方程式:
⑴二氧化氮和水反应:;
⑵碳和浓硝酸共热:;
⑶铜和稀硝酸反应:;
某同学设计了一种电解法制取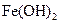 的实验装置(如
的实验装置(如 图)。玻璃管内的电解液为
图)。玻璃管内的电解液为 溶液,通电后,溶液中产生白色沉淀,且较长时间不变色。回答下列问题:
溶液,通电后,溶液中产生白色沉淀,且较长时间不变色。回答下列问题:
(1)写出A电极的电极反应式_________;B电极的电极反应式__________;
(2)若电解改用 溶液作电解液,发现电解一开始即出现灰绿色沉淀试分析为什么用
溶液作电解液,发现电解一开始即出现灰绿色沉淀试分析为什么用 溶液作电解液时白色沉淀能保持较长时间的原因_____________。
溶液作电解液时白色沉淀能保持较长时间的原因_____________。