【改编】用NA表示阿伏伽德罗常数的值。下列叙述不正确的是
| A.标准状况下,22.4LCH4中含有4NA个C-H键 |
| B.48gO2与O3的混合气体中含有3NA个氧原子 |
| C.标准状况下,2.24L氯气溶于水转移的电子数为0.1NA |
| D.1L0.1mol/LFeCl3溶液完全水解得到的Fe(OH)3胶体微粒数小于0.1NA |
在一定条件下,一定量的A和B气体发生如下可逆反应: 2A(g)+3B(g) 3C(g),只有反应到达平衡时才具有的性质是
3C(g),只有反应到达平衡时才具有的性质是
A.各物质的浓度之比为2:3:3
B.混合物各物质浓度的浓度相等
C.A、B、C三种物质的浓度不随时间变化而变化
D.ν(A)、ν(B)、ν(C) 之比为2:3:3
下列不能证明氯的非金属性比硫强的实验是
| A.HCl比H2S稳定 |
| B.HCl溶液(盐酸)的酸性比H2S溶液(氢硫酸)的酸性强 |
| C.HClO4溶液的酸性比H2SO4的酸性强 |
| D.氯气比硫有更强的氧化性 |
N2H4是一种高效清洁的火箭燃料。0.25 mol N2H4(g)完全燃烧生成氮气和气态水时,放出133.5 kJ热量。则下列热化学方程中正确的是
| A.1/2 N2H4(g)+ 1/2 O2(g)= 1/2 N2(g)+ H2O(l)△H=+257kJ·mol-1 |
| B.N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=-133.5kJ·mol-1 |
| C.N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=+534kJ·mol-1 |
| D.N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534kJ·mol-1 |
下列各组物质汽化或熔化,所克服的微粒间的作用力,属于同种类型的是
| A.碘单质的升华和金刚石的熔化 | B.二氧化硅和氯化钾的熔化 |
| C.氧化铝和冰的熔化 | D.苯和液氯的汽化 |
下列装置或操作能达到实验目的的是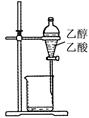
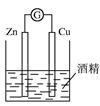
| A.除去乙醇中的乙酸 | B.形成原电池 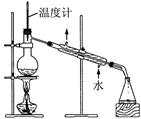 |
| C.制取乙酸乙酯 | D.石油的蒸馏 |