常温下,对pH=10的NaHCO3溶液中,各微粒的物质的量浓度分析正确的是
| A.c(CO32—)>c(H2CO3) |
| B.c(Na+)>c(HCO3—)>c(OH―)>c(H+) |
| C.c(Na+)+c(H+)=c(HCO3—)+c(CO32—)+c(OH―) |
| D.c(Na+)=c(HCO3—)+c(CO32—)+c(H2CO3) |
下列四种溶液中①pH=0的盐酸 ②0.1mol/L的盐酸 ③0.01mol/L的NaOH溶液 ④pH=14的NaOH溶液,由水电离生成的H+浓度之比①:②:③:④是
| A.1:10:100:1 | B.1:10—1:10—12:10—14 |
| C.14:13:12:14 | D.14:13:2:1 |
下列溶液中一定呈中性的是
| A.pH=7的溶液 |
| B.由强酸、强碱等物质的量反应得到的溶液 |
| C.c(H+)=c(OH—)的溶液 |
| D.非电解质溶于水得到的溶液 |
对室温下pH相同、体积相同的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是
| A.加适量的醋酸钠晶体后,两溶液的pH均增大 |
| B.使温度升高20℃后,两溶液的pH均不变 |
| C.加水稀释2倍后,两溶液的pH均减小 |
| D.加足量的锌充分反应后,两溶液中产生的氢气一样多 |
下列现象与电化学腐蚀无关的是
| A.黄铜(铜锌合金)制作的铜锣不易产生铜绿 |
| B.生铁比软铁芯(几乎是纯铁)容易生锈 |
| C.铁质器件附有铜质配件,接触处容易生铁锈 |
| D.银质奖牌放置久了表面变暗 |
实验室使用pH传感器来测定Na2CO3和NaHCO3混合物中NaHCO3的含量。称取1.59 g 样品,溶于水配成250 .00 ml溶液,取出该溶液25.00 ml用 0.1 mol·L-1盐酸进行滴定,得到如下曲线。以下说法或操作正确的是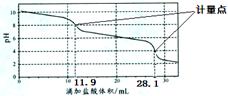
| A.上一个计量点前发生反应的离子方程式为HCO3-+H+===H2O+CO2↑ |
| B.下一个计量点溶液中存在大量的阴离子是Cl-、HCO3- |
| C.此样品n(NaHCO3)=" (28.1" - 2×11.9)×10-4 mol |
| D.使用该方法测定Na2CO3和NaOH混合溶液中的氢氧化钠含量,将会得到1个计量点 |