(15分)亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。工业设计生产NaClO2的主要流程如下:

(1)A的化学式是 ,装置III中A在 极区产生。
(2)II中反应的离子方程式是 。
(3)通电电解前,检验III中阴离子的方法和步骤是 。
(4)为防止II中制备的NaClO2被还原成NaCl,应选合适的还原剂,除双氧水外,还可以选择的还原剂
是 (填字母编号)。
a.Na2O2 b.FeCl2 c.Na2S
(5)气体a、b与氢氧化钠溶液可构成燃料电池,用该电池电解200 mL 0.5 mol·L-1的CuSO4溶液,生成铜3.2 g,此时所得溶液中离子浓度由大到小的顺序是 。
亚硝酸钠是一种工业盐,在生产、生活中应用广泛。现用下图所示仪器(夹持装置已省略)及药品,探究亚硝酸钠与硫酸反应及气体产物成分。
已知:①NO+NO2+2OH-=2NO2-+H2O;②气体液化的温度:NO2 21℃、NO–152℃。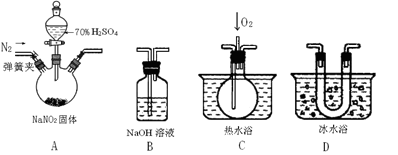
(1)为了检验装置A中生成的气体产物,仪器的连接顺序(按左→右连接): A、、、。
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是。
(3)在关闭弹簧夹,打开分液漏斗活塞,滴入70%硫酸后,A中产生红棕色气体。
①确认A中产生的气体含有NO,依据的现象是。②装置D的作用是。
(4)如果向C中通入过量O2,则装置B中发生反应的总化学方程式为。
(5)通过上述实验探究过程,可得出装置A中反应的化学方程式是。
某化学兴趣小组欲制取氨气和氯化氢气体并完成喷泉实验(图中夹持装置均已略去)。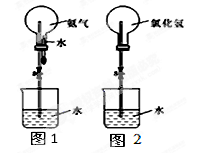
(1)写出实验室制取氨气的化学方程式:。
(2)收集氯化氢气体应使用法,要得到干燥的氨气可选用作干燥剂。
(3)如果用图1装置进行喷泉实验,上部烧瓶已装满干燥氨气,打开止水夹,挤出胶头滴管中的水引发水上喷。该实验的原理 是。
(4)如果用图2装置进行喷泉实验,上部烧瓶已装满干燥氯化氢气体,请说明引发喷泉的方法。
(5)若至喷泉实验停止时,图1中剩有烧瓶容积1/5的气体;图2烧瓶中剩有烧瓶容积1/4的气体;则图2烧瓶中盐酸的物质的量浓度为(两种气体均在标准状况下收集);图1烧瓶中氨水的物质的量浓度(填“大于”、“小于”、“等于”)图2烧瓶中盐酸的物质的量浓度。
(8分)氯气是一种重要的化工原料,在生产和生活中应用十分广泛。
已知: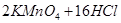 (浓)="==="
(浓)="===" 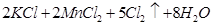 ,在实验室可用二氧化锰固体或高锰酸钾固体和浓盐酸反应制取氯气。可供选用的发生装置如下图。
,在实验室可用二氧化锰固体或高锰酸钾固体和浓盐酸反应制取氯气。可供选用的发生装置如下图。
(1)若用高锰酸钾固体和浓盐酸反应制取氯气,发生装置是。(选填A或B或c)
(2)写出用二氧化锰固体和浓盐酸反应制取氯气的化学方程式:。
(3)实验室收集氯气的方法是。
(4)常用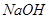 溶液吸收氯气防止污染。写出该反应的离子方程式。
溶液吸收氯气防止污染。写出该反应的离子方程式。
(10分)为测定某含有杂质Na2O的Na2O2样品的纯度,2个小组分别设计如下方案。首先准确称量样品mg,然后,按照以下方案进行实验,请你完成相关内容:
[方案一]:将样品与水充分反应,使产生的O2通过灼热的铜粉,测得反应后生成氧化铜的质量为ng,通过计算求出试样中Na2O2的含量。
(1)Na2O2跟水反应的离子方程式是:;
(2)根据所给数据计算出的试样中Na2O2含量的代数式为 。
[方案二]:将样品与二氧化碳反应,通过测定反应产生氧气的体积,计算出样品中Na2O2的含量。
(1)上图是完成该实验可能用到的实验装置,根据此实验方案,实验所使用仪器的连接次序是。(填写仪器编号)
(2)装置①⑤的作用分别是:①⑤。
二氧化氯(ClO2)是一种高效消毒剂,沸点为11℃。用氯酸钾粉末与草酸在60℃时反应可生成二氧化氯等物质,实验装置如下图所示:
(1)装置A中还应安装的玻璃仪器是____,装置B用冰水浴的原因是________.
(2)装置A中反应产物有K2CO3、ClO2和CO2等,请写出该反应的化学方程式:________________.
(3)①实验过程中,装置C中少量的ClO2与NaOH溶液反应产生两种钠盐,且物质的量之比为1:1,其中一种为NaClO2,写出装置C中生成这两种钠盐的离子方程式:_____________________________。
②饱和溶液在温度低于38℃时析出晶体NaClO2.3H2O,在温度高于38℃时析出晶体NaClO2。请补充从NaClO2溶液中制得NaClO2晶体的操作步骤:
a.____________________;b________________________;c.洗涤;d.干燥。
(4)还可采用盐酸或双氧水还原氯酸钠制备ClO2。用H2O2作还原剂制备ClO2更受欢迎,其主要原因是______________。