科学家设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如下图所示,下列说法不正确的是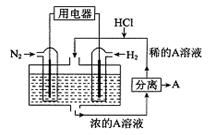
| A.通入N2的电极发生的电极反应式为:N2 + 6e- + 8H+="=" 2NH4+ |
| B.反应过程中溶液的pH会变大,故需要加入盐酸 |
| C.该电池外电路电流从通入H2的电极流向通入N2的电极 |
| D.通入H2的电极为负极,A为NH4Cl |
下列说法中有明显错误的是
| A.升高温度,一般可使活化分子的百分数增大,因而反应速率增大 |
| B.活化分子之间发生的碰撞一定为有效碰撞 |
| C.干冰升华这一过程中,△S>0 |
D.对于反应:CO (g)+H2O (g)  CO2 (g)+H2 (g),恒容时,温度升高,H2浓度增大,则该正反应的焓变为正值 CO2 (g)+H2 (g),恒容时,温度升高,H2浓度增大,则该正反应的焓变为正值 |
化学家庭小实验是利用家庭日常生活用品进行化学学习和探究的活动。下列家庭小实验设计肯定不合理的是
| A.用米汤检验食用加碘盐中是否含碘元素 |
| B.用食醋检验鸡蛋壳中是否含有碳酸盐 |
| C.用食用碱(Na2CO3)溶液洗涤餐具上的油污 |
| D.在自来水中加入明矾起到净水作用 |
下列说法正确的是
| A.如果苯酚溶液沾到皮肤上,应立即用氢氧化钠溶液洗涤 |
| B.重结晶时,溶液冷却速度越慢得到的晶体颗粒越小 |
| C.用新制的Cu(OH)2浊液可以检验牙膏中的甘油 |
| D.将3~4根火柴头浸于水中,片刻后取少量溶液于试管中,加AgNO3溶液和稀HNO3,可以检验火柴头中的氯元素 |
关于强电解质和弱电解质的说法正确的是
| A.强电解质溶液的导电能力一定比弱电解质溶液强 |
| B.强电解质的水溶液中不存在分子 |
| C.弱电解质的水溶液中既存在分子又存在自由移动的离子 |
| D.因为NH3·H2O是弱电解质,所以在AlCl3溶液中加入氨水不能制取Al(OH)3沉淀 |
相同条件下,同浓度的下列溶液,其pH值最大的是
| A.Na2CO3 | B.CH3COONa | C.NaCl | D.NaHSO4 |