粗盐中除NaCl外还含有MgSO4以及泥沙等杂质。初步提纯粗盐的实验流程如下:
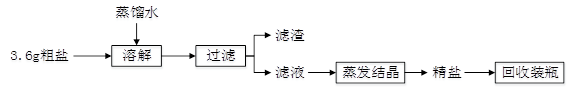
(1)“滤渣”是粗盐中含有的 。
(2)实验过程中四次用到玻璃棒,分别是:
第一次:溶解时搅拌;
第二次: ;
第三次: ;
第四次:将精盐从蒸发皿转移出来。
(3)本实验从滤液得到精盐,采用的是蒸发溶剂的方法而不用降低溶液温度的方法,参考溶解度曲线图分析的原因:

(4)看图可知,200C时NaCl的溶解度为 g,本实验溶解3.6g的粗盐,蒸馏水的最佳使用量约为 ml.增加蒸馏水的用量虽然能加快粗盐的溶解,但会引起的不良后果是 。
实验是科学探究的重要手段。如图是实验室制取气体的常用装置,请回答有关问题:

(1)仪器①的名称 。实验室利用高锰酸钾制取氧气的装置中,试管口略向下倾斜的原因是 。
(2)实验室里,在常温下用硫化亚铁固体和稀硫酸反应来制取硫化氢气体。通常情况下,硫化氢是一种无色、有臭鸡蛋气味的有毒气体,能溶于水,密度比空气的大。实验室制取硫化氢气体应选用的发生装置是 (填序号),收集装置是 (填序号)。
化学实验是进行科学探究的重要途径。某研究性学习小组欲利用下列装置进行相关气体制取的探究,请你分析并回答问题:

(1)图中标号a的仪器名称是 。
(2)若用加热高锰酸钾固体制取并收集一集气瓶氧气,可选用的装置组合是 (填字母序号)。
(3)实验室用过氧化氢溶液和二氧化锰制取氧气的化学方程式为 。主要操作步骤有:①检查装置的气密性;②收集并验满气体;③装入药品;④组装仪器。正确的操作顺序是 (填数字序号)。
(4)F是密封良好充满空气的单气阀充气袋,现用F收集一袋较纯净的氧气,则导气管口b、c连接之前需进行的一项操作是 。
如图是某果蔬洗涤盐说明书。小明对配料表中的成分很好奇:食盐可用于杀菌消毒,为什么要加入pH调节剂,它的成分是什么?
【查阅资料】1.该品牌果蔬洗涤盐pH调节剂的成分可能是碳酸钠、碳酸氢钠、酒石酸、柠檬酸中的一种或两种。pH调节剂能维持渗透压、控制酸碱平衡。
2.大多数农药是酸性的。
3.碳酸氢钠加热易分解,碳酸钠则有较高的热稳定性,二者的溶液都显碱性。
【实验初探】取少量该固体溶于水配成溶液A。用pH试纸测得该溶液的pH=10,该洗涤盐溶液显 性,则pH调节剂中一定不含的物质是 。
【猜想与假设】该配料表中的pH调节剂可能是①碳酸钠;②碳酸氢钠;③ 。
【实验再探】
|
序号 |
实验操作 |
实验现象 |
实验结论 |
|
(1) |
取少许A溶液于试管中,滴加氯化钙溶液 |
有白色沉淀生成 |
|
|
(2) |
取适量洗涤盐,加热,将生成的气体通入澄清石灰水 |
观察到 |
证明该pH调节剂中含有碳酸氢钠。 |
【分析与结论】猜想③正确
【反思与评价】请你从1,2中任选一题回答。
1.你认为果蔬洗涤盐中pH调节剂的作用是什么? 。(答一条即可)
2.该商品配料表中有一处表述不恰当,请你改正过来 。

氧气和二氧化碳的制取和性质是初中化学的重要内容。根据下列所示的装置回答问题。

(1)请写出用A装置制取氧气的化学方程式 。若用B、C装置制取氧气,以下操作①装药品并固定装置;②检查装置气密性;③熄灭酒精灯;④加热;⑤收集气体;⑥将导气管移出水槽,正确的操作顺序是 (用序号表示)。若将红热的铁丝伸入制得的氧气中,现象是 。
(2)要制取一瓶干燥的二氧化碳,应选择的装置是 (用装置序号表示),将干燥的 分别通入G、H中,G中试纸不变色、H中试纸变红色。请用化学方程式表示H中试纸变红的原因 。
2021年12月9日,由航天员王亚平主讲的“天宫课堂”压轴实验圆满成功。实验中往漂浮在空中蓝色水球中放入半片泡腾片【主要成分是柠檬酸( )和碳酸氢钠】,泡腾片与水作用,不断产生小气泡,水球逐渐变大。产生的气泡是什么呢?为什么泡腾片遇到水才产生气泡?
【猜想与假设】
小亮同学结合已有知识,判断产生的气泡是 ,他的判断依据是 。
【设计并进行实验】
小亮同学在实验室利用以下装置,模拟用维生素C泡腾片和水制取并验证该气体的性质。

(1)仪器a的名称 ;仪器b的名称 。
(2)实验室要用以上装置制取并收集该气体。需要选择的发生装置和收集装置是 (填序号),选择此发生装置的依据是 。
(3)小亮同学将该气体通入到盛有澄清石灰水的试管中,观察到的现象是 ,请写出此反应的化学方程式 ,证明该气体是二氧化碳。
【反思交流】
小丽同学提出,泡腾片遇到其他液体也能产生气泡吗?她设计并进行了以下4个实验,将4片同样的泡腾片同时放入四个盛有50mL不同液体的烧杯中:
|
实验 |
实验现象 |
实验结论 |
|
|
实验1 |
放入水中 |
水中有大量气泡产生; |
有水存在,泡腾片才能产生 。 |
|
实验2 |
放入植物油中 |
植物油中 ; |
|
|
实验3 |
放入酒精中 |
酒精中无明显现象; |
|
|
实验4 |
放入白醋中 |
白醋中 。 |
|
设置实验1的目的是 ,通过以上实验你还得出的结论是 。
【实验启示】
维生素C泡腾片最好 保存。