现有一定质量含有少量泥沙等不溶性杂质和少量Na2SO4,MgCl2,CaCl2等可溶性杂质的粗盐样品,某实验小组利用化学实验室常用仪器对粗盐样品进行提纯,提纯步骤如下:
请根据提纯步骤回答下列问题.
(1)步骤⑦的操作名称为 .
(2)请写出实验步骤②中所涉及的化学方程式 .
(3)步骤⑥中加入过量盐酸的目的是 .
(4)步骤②和步骤④ (填“可以”或“不可以”)颠倒,理由是 .
(5)检验步骤④中Na2CO3溶液已过量的方法是 .
(6)加碘食盐相关信息如图所示.

食盐中的碘酸钾(KIO3)在酸性条件下,可以将碘化钾(KI)变成碘(I2),化学方程式如下:
KIO3+5KI+6HCl=6KCI+3I2+3H2O
①向装有碘化钾和淀粉混合液的试管中,滴入稀盐酸将溶液酸化,再加入食盐,若食盐中有碘化钾,则加入食盐后的实验现象 .
②小强同学欲测定加碘盐中碘元素的质量分数,实验步骤如下:取10g食盐样品于试管中加水溶解,加入过量KI的和淀粉混合溶液,再滴入稀盐酸将溶液酸化使其充分反应后,调节溶液呈中性,再向试管中滴加硫代硫酸钠溶液(Na2S2O3),发生化学反应方程式为:2Na2S2O3+I2═Na2S4O6+2NaI
当加入质量分数为0.237%Na2S2O3溶液2g时,I2恰好反应完全,通过计算判断该食盐样品是否合格(已知Na2S2O3的相对分子质量为158.请写出计算过程).
化学实验是学习化学的重要方法.请完成下列金属性质的实验
(1)实验一:比较铁、铜的金属活动性强弱,请你设计实验完成下表内容。
| 实验步骤 |
实验现象 |
结论 |
| 金属活动性:Fe>Cu |
(2)实验二:镁、锌、铁三种金属与酸的反应。
[实验]取一定量的镁、锌、铁三种金属分别加入到溶质质量分数相同的稀硫酸中,充分反应,观察现象。
[结论]活泼金属能与酸反应。
[分析]①三个反应的共同特点是 ,写出其中一个反应的化学方程式 。
②若完全反应后,三个反应生成氢气的质量相等,原因是 。
如图所示,取三根粗细、长度均相同的光亮细铁丝,将其中两根分别盘成螺旋状,在每根铁丝一端绑上粗铜丝,另一端系一火柴,点燃火柴,待快燃尽时,分别插入充满氧气的集气瓶中(预先放入一些水).观察到:I、II中铁丝都剧烈燃烧,且II中铁丝燃烧比I中的更剧烈;III中铁丝没有燃烧。
(1)为什么III中铁丝不能燃烧?
(2)分析II中铁丝燃烧比I中的更剧烈的原因。
如图是某同学设计的实验室制取二氧化碳并验证其性质的实验装置图.
请回答下列问题:
(1)将A、E装置连接时,应将A装置的导管a与E装置的导管 (选填“b”或“c”)相连接.检验E装置中二氧化碳已收集满的方法是 .
(2)将A、B装置连接,观察到的现象是 ,可验证二氧化碳的性质是 .
(3)将A、C装置连接,可验证二氧化碳与氢氧化钙反应,该反应的化学方程式为: .
(4)用E装置收集一瓶二氧化碳气体,取下双孔橡皮塞,将瓶中的气体沿D装置烧杯左侧内壁缓慢倒入,观察到的现象时 ,这些现象说明二氧化碳具有的物理性质 ,化学性质 , .
实验室内有一瓶化肥的标签已脱落,只知道它是NH4Cl、(NH4)2SO4和KNO3中的一种.现进行如下实验:
(1)取少量样品在研钵中与 混合研磨,有刺激性气味的气体放出.
(2)另取少量化肥样品与试管中,加入少量水溶解,再滴入图中的 溶液,产生白色沉淀.根据以上实验,可知该化肥为 .
硫酸铜晶体常用作农业和渔业的杀虫剂、杀菌剂,某同学设计了下列两条途径由废铜料(含铁)生产硫酸铜晶体,其过程如下所示: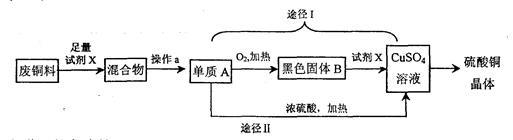
(1)操作a的名称是: ;
(2)已知:Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O。则途径I与途径II相比,其优点体现在:
①不产生二氧化硫有毒气体,不会污染空气;② ;
(3)将废铜料投入硫酸铜溶液中充分搅拌,发生反应的化学方程式为: 。