实验室模拟“侯氏制碱法”制纯碱,其原理是NaCl+NH4HCO3=NaHCO3+NH4Cl,再将碳酸氢钠加热分解得到纯碱。下图是NaCl、NH4Cl、NaHCO3的溶解度曲线,下列说法正确的是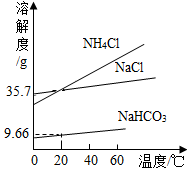
| A.NaHCO3从溶液中分离出,可采用的操作是蒸发结晶 |
| B.NH4Cl饱和溶液的溶质质量分数一定大于NaCl饱和溶液的溶质质量分数 |
| C.40℃时,溶解度大小关系是:NH4Cl>NaCl>NaHCO3 |
| D.20℃时,100g水中加入11.7g NaCl和15.8g NH4HCO3固体,充分反应后,理论上可析出7.14g NaHCO3晶体 |
下列实验能达到目的的是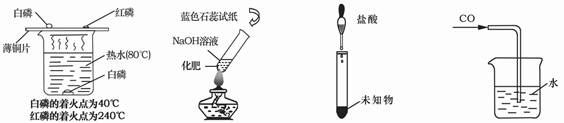
①②③④
| A.①验证可燃物燃烧的条件 | B.②检验铵态氮肥 |
| C.③检验CO32一的存在 | D.④用水吸收CO |
下列比较金属活动性强弱的实验设计、现象和结论均正确的是
| 选项 |
实验设计 |
现象 |
结论(金属的活动性) |
| A |
将铝丝放人硫酸铜溶液中 |
无现象 |
Cu>Al |
| B |
分别将相同形状的镁条和铝条点燃放入盛氧气的集气瓶中 |
镁条燃烧得更剧烈 |
Mg>Al |
| C |
分别将锌粉与铁丝放入相同浓度的稀盐酸中 |
锌粉产生气泡的速率比铁丝快 |
Zn>Fe |
| D |
分别将铁丝与铜丝放入相同浓度的稀盐酸中 |
铁丝表面产生气泡,铜丝无现象 |
Fe>Cu |
根据下表提供的信息,下列判断正确的是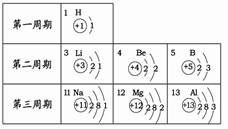
| A.元素所在的周期数等于其原子的电子层数 |
| B.钠离子核外有三个电子层 |
| C.第二、三周期元素的原子从左至右最外层电子数逐渐增多 |
| D.在化学变化中镁元素容易失去最外层2个电子形成镁离子,其离子符号是Mg+2 |
物质的性质决定其用途。下列有关物质性质和用途的说法中错误的是
| A.烧碱显碱性——可以中和酸性土壤 |
| B.氮气性质比较稳定——可充人食品包装袋中防腐 |
| C.铜片能导电——可作电极 |
| D.干冰升华吸收热量——可用于人工降雨 |
下列有关溶液及其性质的说法中错误的是
| A.海水的凝固点比水低 |
| B.溶液和浊液特征的不同主要与物质分散在液体中的颗粒大小有关 |
| C.一定温度下,物质的溶解度随水的量的变化而变化 |
| D.食盐水能导电是因为食盐水中含有较多自由移动的离子 |