石灰石样品的主要成分是CaCO3(已知其它杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象:
| 次数 |
第1次 |
第2次 |
第3次 |
| 加入盐酸的质量/g |
10 |
10 |
10 |
| 剩余固体的质量/g |
16 |
12 |
8 |
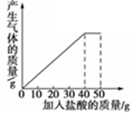
请计算:
(1)石灰石样品中杂质的质量为 g。
(2)所加盐酸的溶质质量分数.
实验室用过氧化氢溶液(过氧化氢与水的混合物)与二氧化锰混合制取氧气.现将50g过氧化氢溶液和1g二氧化锰混合物放入锥形瓶中,完全反应结束后,称得锥形瓶中剩余物质的质量为47.8g。
计算:(1)完全反应后产生氧气的质量为______g.
(2)过氧化氢溶液中过氧化氢的质量分数
湿法冶金是我国古代劳动人民智慧的结晶。向一定质量含杂质的铁粉中(假设杂质不溶于水,也不与其他物质反应)加入一定质量硫酸铜溶液(含l6g硫酸铜),铁与硫酸铜均恰好完全反应后,过滤、干燥得到6.8g固体。试求原铁粉的质量分数。
N(NO2)3是科学家于2011年发现的一种新型火箭推进剂的原料。请计算:
(1)N(NO2)3是由种元素组成。
(2)N(NO2)3分子中氮、氧原子的个数比。
(3)N(NO2)3中氮、氧元素的质量比是。
(4)N(NO2)3中氮元素的质量分数是。
(5)304gN(NO2)3含氮元素的质量为。
实验室需要氧气做实验。现将24.5 g氯酸钾和5.5克二氧化锰的混合物放入试管中加热完全分解,试计算:
(1)制得氧气的质量(2)完全反应后试管中剩余固体物质有哪些?各为多少g?
香椿被称为“树上蔬菜”,是香椿树的嫩芽,它不仅营养丰富,且具有极高的药用价值,如香椿中含有的皂甙具有抗菌、防癌的作用,皂甙的化学式为C27H42O3,请你计算:
(1)皂甙由种元素组成;每个分子中有个原子。
(2)皂甙中碳元素和氧元素的质量比为。
(3)207g皂甙中有多少g碳元素。