在一定温度下,将2mol A和2molB 两种气体相混合于容积为2L的某密闭容器中,发生如下反应:3A(g)+B(g) xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8mol D,并测得C的浓度为0.4 mol·L-1,试求:
xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8mol D,并测得C的浓度为0.4 mol·L-1,试求:
(1)x值
(2)B的平衡浓度
(3)A的转化率
(4)用A表示的化学反应速率
一定量的某有机物与NaOH的醇溶液共热,产生的气体在标准状况下为896 mL,同时得溶液100 mL,取出10 mL溶液先用HNO3酸化后再加入AgNO3溶液直到不再产生白色沉淀为止,用去0.1 mol·L-1AgNO3溶液40 mL,所得气体完全燃烧时消耗O2 0.18 mol,试确定该有机物的结构简式和名称。
标准状况下1.68 L无色可燃气体在足量氧气中完全燃烧。若将产物通入足量澄清石灰水,得到的白色沉淀质量为15.0 g;若用足量碱石灰吸收燃烧产物,增重9.3 g。
(1)计算燃烧产物中水的质量。
(2)若原气体是单一气体,通过计算推断它的分子式。
(3)若原气体是两种等物质的量的气体的混合物,其中只有一种是烃,请写出它们的分子式(只要求写出一组)。
将128 g铜置入一定量的浓硝酸中,并微热,随着铜的不断减少,反应生成的气体颜色逐渐变浅,当铜反应完毕时(铜片完全消失),共收集到NO2和NO的混合气体44.8 L气体(标准状况),求:
(1)写出上述过程中,有关反应的化学方程式___________、_________________。
(2)完成该反应至少需要量取10 mol/L的浓硝酸_________mL。
(3)混合气体中NO2的体积为 、NO的体积为 。
把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入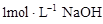
溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。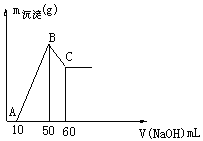
(1)合金中镁的质量g铝的质量g
(2)盐酸的物质的量浓度mol/L
将15.6 g Na2O2投入到足量的水中充分反应。回答:
(1)生成的气体在标准状况下的体积为L。
(2)该反应中所消耗的水的质量为g。
(3)将反应后的溶液配成1000mL溶液,所得溶液的物质的量浓度为mol·L-1。