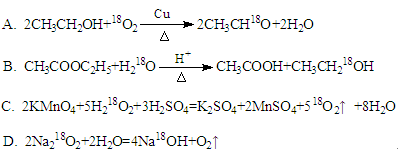已知某溶液中含有下列8种离子中的5种(忽略水的电离及离子的水解):K+、Cu2+、Al3+、Fe2+、Cl-、CO32-、NO3-、SO42-,且5种离子的物质的量浓度相等。为了进一步探究该水溶液的组成,某同学进行了如下实验:
①用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃观察无紫色火焰。
②另取溶液加入足量盐酸,有无色气体生成,该无色气体遇空气变成红棕色。
③另取溶液加入BaCl2溶液,有白色沉淀生成。
根据上述实验,以下推测正确的是____。
| A.无法确定溶液中是否存在Cu2+离子 |
| B.原溶液中不含K+、Al3+、CO32-等离子 |
| C.根据步骤②只能确定溶液中一定存在NO3-离子 |
| D.步骤③所得到的白色沉淀共有2种钡盐 |
下列各组物质中,一定互为同系物的一组是
| A.C3H6与C5H10 | B.C3H8与C5H12 |
| C.分子式为CH4O和C2H6O的物质 | D.苯酚和苯甲醇(C6H5CH2OH) |
下列叙述:①中国科学家于1965年首次人工合成了具有生物活性的蛋白质——结晶牛胰岛素;②瑞典化学家贝采利乌斯首次提出了“有机化学”的概念;③德国化学家维勒首次人工合成了有机物——尿素;④德国化学家李比希首创了有机物的定量分法方法和“基团”理论。其中正确的是
| A.① | B.①③ | C.①②③ | D.①②③④ |
(共13分)从薄荷油中得到一种烃A(C10H16),叫α-非兰烃,与A相关反应如下: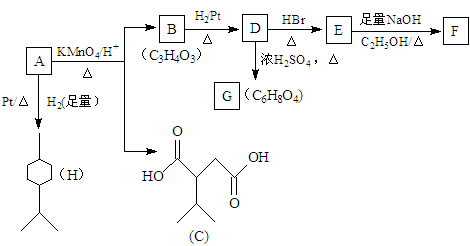

(即碳碳双键的碳原子上若有一个氢原子,氧化后形成羧基,若无氢原子,则氧化后生成羰基)
(1)D→E的反应类型为。
(2)B所含官能团的名称为。
(3)G为含六元环的化合物,写出其结构简式。
(4)F在一定条件下发生聚合反应可得到一种高吸水性树脂,该树脂的链节为。
(5)写出E→F(已知F的分子式C3H3O2Na)的化学方程式。
(6)A与Br2加成后的可能产物共有种(不考虑立体异构)
(7)C的同分异构体有多种,写出一种满足下列条件的同分异构体的结构简式。
①含两个—COOCH3基团
②核磁共振氢谱呈现2个吸收峰
某有机物A的结构如图所示,下列叙述正确的是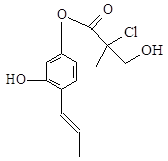
| A.1molA最多可4molBr2发生反应 |
| B.A分子中含有三类官能团 |
| C.1molA与足量的NaOH溶液反应,最多消耗3molNaOH |
| D.A的分子为C13H15O4Cl |
同位素示踪法可用于反应机理的研究。下列反应同位素示踪表示正确的是