【改编】含有一定量NaOH溶液中,逐渐通入一定量CO2,充分反应后,将溶液在一定条件下进行低温蒸干,得到晶体物质。其质量m 与通入气体体积V(CO2)的关系如图。如下说法正确的是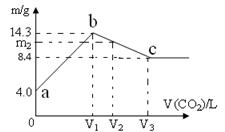
| A.整个过程中的溶液,一定存在恒等式:]c(Na+)+c(H+)=c(OH-)+c(CO32-)+c(HCO3-) |
| B.晶体物质:a点是NaOH,b点是Na2CO3 |
| C.c点的溶液中存在c(OH-)-c(CO32-)= c(H+)+c(H2CO3) |
| D.若通入V2="1.344" L (标况)气体,则m2="13.12" g |
下列物质:①H3O+;②[B(OH)4]-;③CH3COO-;④NH3;⑤CH4中存在配位键的是( )
| A.①② | B.①③ | C.④⑤ | D.②④ |
在标准状况下,在三个干燥的烧瓶内分别装入:纯净的NH3,含有少量空气的NH3,NO2和O2的混合气体[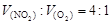 ]。然后分别做喷泉实验,三个烧瓶中所得溶液的物质的量浓度之比为( )
]。然后分别做喷泉实验,三个烧瓶中所得溶液的物质的量浓度之比为( )
| A.21︰12︰4 | B.5︰5︰4 | C.5︰5︰1 | D.无法确定 |
将100mL 1mol/L的NaHCO3溶液等分为两份,其中一份加入少许冰醋酸,另外一份加入少许Ba(OH)2固体,忽略溶液体积变化,两份溶液中 的变化分别是( )
的变化分别是( )
| A.减小、减小 | B.减小、增大 | C.增大、增大 | D.增大、减小 |
下列有关物质的性质与应用不相对应的是( )
| A.明矾能水解生成Al(OH)3胶体,可用作净水剂 |
| B.FeCl3溶液能与Cu反应,可用于蚀刻印刷电路 |
| C.SO2具有氧化性,可用于漂白纸浆 |
| D.Zn具有还原性和导电性,可用作锌锰干电池的负极材料 |
短周期元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族。下列叙述正确的是( )
| A.元素X的简单气态氢化物的热稳定性比W的弱 |
| B.元素W的最高价氧化物对应水化物的酸性比Z的弱 |
| C.化合物YX、ZX2、WX3中化学键的类型相同 |
| D.原子半径的大小顺序:Y>Z>W>X |