下表中的实验操作能达到实验目的或能得出相应结论的是
| 选项 |
实验操作 |
实验目的或结论 |
| A |
向一定浓度的Na2SiO3溶液中通入适量CO2气体 |
H2SiO3的酸性比H2CO3的酸性强 |
| B |
取少量KClO3晶体溶于适量的蒸馏水,再加入硝酸酸化的AgNO3溶液 |
检验KClO3中的氯元素 |
| C |
向某溶液中滴加Ba(NO3)2溶液产生白色沉淀,再加稀盐酸沉淀消失 |
说明原溶液中一定含有CO32—或 SO32— |
| D |
将混有Ca(OH)2杂质的Mg(OH)2样品,放入水中搅拌成浆状后,加入足量饱和氯化镁溶液充分搅拌、过滤,沉淀用蒸馏水洗涤 |
除去Mg(OH)2样品中的Ca(OH)2 |
下列有机物的名称一定错误的是( )-
| A.2一甲基一1一丁烯 |
| B.2,2一 二甲基丙烷 |
| C.5,5一二甲基一3一己烯 |
| D.4一甲基一2一戊炔 |
下列说法正确的是( )
| A.乙炔的结构简式为CHCH |
| B.羟基(一OH)和氢氧根(OH一)的电子数不同 |
C.对甲基苯甲醛的结构简式为 |
D. 与 与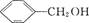 互为同系物 互为同系物 |
下列根据操作和现象或目的所得出的结论正确的是
| 选项 |
操作 |
现象或目的 |
结论 |
| A |
工业上,将BaSO4浸泡在饱和Na2CO3溶液中 |
将BaSO4转化为BaCO3 |
Ksp(BaSO4)>Ksp(BaCO3) |
| B |
向NaAlO2溶液中滴入NaHCO3 |
有白色沉淀 |
AlO结合H+能力比CO强 |
| C |
向PbO2中滴入浓盐酸 |
有黄绿色气体 |
PbO2具有还原性 |
| D |
向鸡蛋白溶液中滴入HgCl2溶液 |
有白色沉淀 |
蛋白质发生盐析 |
菠萝酯常用作化妆品香料,其合成方法如下: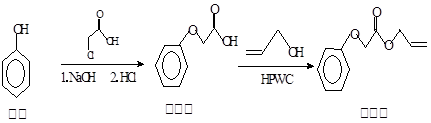
下列说法正确的是
| A.原料苯酚能和NaHCO3溶液反应 |
| B.菠萝酯可以使溴水、高锰酸钾溶液褪色 |
| C.中间体中所有的原子都可以共平面 |
| D.中间体和菠萝酯中均不含手性碳原子 |
下列有关说法正确的是
| A.一定条件下,使用催化剂能加快反应速率但不能改变平衡转化率 |
| B.氢氧燃料电池的能量转换形式仅为化学能转化为电能 |
| C.在NH4HSO4溶液中由于NH4+的水解促进了水的电离,所以水的电离程度增大 |
D.在一密闭容器中发生2SO2+O2 2SO3反应,增大压强,平衡会正向移动, 2SO3反应,增大压强,平衡会正向移动,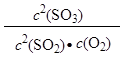 的值增大 的值增大 |