下列叙述中因果关系成立的是
| A.因为NH3的水溶液可以导电,所以NH3是电解质 |
| B.因为SO2可以使溴水褪色,所以SO2具有漂白性 |
| C.因为加热后纯水的pH<7,所以升温可使水呈酸性 |
| D.因为电解质溶于水后发生电离,所以电解质在溶液中的反应实质是离子间的反应 |
某消毒液的主要成分为NaClO,还含有一定量的NaOH。下列用来解释事实的方程式中,不合理的是(已知:饱和NaClO溶液的pH约为11) ( )
| A.该消毒液可用NaOH溶液吸收Cl2制备:Cl2+2OH-=ClO-+Cl-+H2O |
B.该消毒液的pH约为12:ClO-+H2O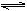 HClO+OH- HClO+OH- |
| C.该消毒液与洁厕灵(主要成分为HCl)混用,产生有毒Cl2:2H++Cl-+ClO-=Cl2↑+H2O |
| D.该消毒液加白醋生成HClO,可增强漂白作用:CH3COOH+ClO-=HClO+CH3COO- |
用下图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的
是()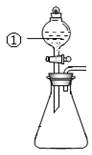
| 选项 |
①中物质 |
②中物质 |
预测②中的现象 |
| A. |
稀盐酸 |
碳酸钠与氢氧化钠的混合溶液 |
立即产生气泡 |
| B. |
浓硝酸 |
用砂纸打磨过的铝条 |
产生红棕色气体 |
| C. |
氯化铝溶液 |
浓氢氧化钠溶液 |
产生大量白色沉淀 |
| D. |
草酸溶液 |
高锰酸钾酸性溶液 |
溶液逐渐褪色 |
下列离子在指定条件下能大量共存的是 ( )
| A.能使石蕊试液显红色的溶液中:NH4+、Fe 2+、Al3+、NO3- |
| B.加入NH4HCO3能产生气体的溶液中:K+、Na+、I-、SO42- |
| C.中性透明溶液中:K+、HCO3-、NO3-、Fe3+ |
| D.常温下由水电离出的c(H+)•c(OH-)=10-20的溶液中:Na+、NH4+、Cl-、SiO32- |
下列说法正确的是 ( )
| A.I的原子半径大于Br,HI比HBr的热稳定性强 |
| B.P的非金属性强于Si,H3PO4比H2SiO3的酸性强 |
| C.Al2O3和MgO均可与NaOH溶液反应 |
| D.SO2和SO3混合气体通入Ba(NO3)2溶液可得到BaSO3和BaSO4 |
设NA为阿伏加德罗常数的值,下列说法正确的是()
| A.2.0gH218O与D2O的混合物中所含中子数为NA |
| B.1mol Na2O2固体中含离子总数为4 NA |
| C.标准状况下,5.6LCO2与足量Na2O2反应转移的电子数为0.5 NA |
| D.50ml 12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA |