用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.5.6g Fe和足量的盐酸反应时,失去的电子数为0.3NA |
| B.1molNa2O2固体中含离子总数为3NA |
| C.标准状况下,22.4 L SO3所含分子数为NA |
| D.0.5mol/L的MgCl2溶液中,含有Cl-个数为NA |
下列关于实验仪器和用品的选择,不正确的是 ()
| A.实验室制备乙烯时加入碎瓷片,可以防止暴沸 |
| B.用KMnO4滴定H2C2O4时需要用到两支酸式滴定管 |
| C.进行中和热的测定实验时,必须用到两个量筒和两个温度计 |
| D.实验室测定化学反应速率时,需要用到仪器秒表 |
从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平。下图表示了三种金属被人类开发利用的大致年限,之所以有先后,主要取决于 ()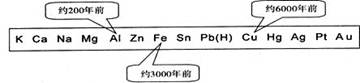
| A.金属的密度大小 | B.金属的活动性大小 |
| C.金属的用途大小 | D.金属在地壳中的含量多少 |
据报道,纳米Fe3 O4晶体材料可以作为核磁共振造影增强剂 ,用于疾病的诊断和作为药物载体用于疾病的治疗。其制备过程如图所示、下列叙述不合理的是 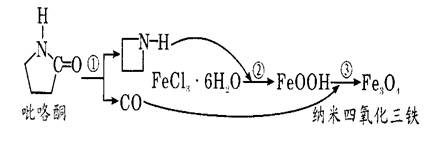
| A.Fe3O4可以表示为 FeO·Fe2O3,属于混合物 | |
B.反应③的化学方程式是:6FeOOH + CO ==2Fe3O4+3H2O+CO2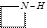 |
C.纳米四氧化三铁分散在适当分散剂中,形成的分散系可能有丁达尔现象 |
| D.在反应②环丙胺的作用可能是促进氯化铁水解 |
从下列事实所得出的相应结论正确的是()
| 实验事实 |
结论 |
|
| ① |
 的水溶液可以导电 的水溶液可以导电 |
 是电解质 是电解质 |
| ② |
将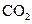 通入到 通入到 溶液中产生白色浑浊 溶液中产生白色浑浊 |
酸性: |
| ③ |
 溶液与 溶液与 溶液混合产生白色沉淀 溶液混合产生白色沉淀 |
酸性: |
| ④ |
常温下白磷可自燃而氮气须在放电时才与氧气反应 |
非金属性: |
| ⑤ |
某无色溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝 |
该溶液一定有 NH4+ |
| A.③④⑤ | B.②③⑤ | C.①②③ | D.全部 |
设NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.1L 0.1 mol·L-1的CH3COONa溶液中CH3COO-的总数是0.1NA |
| B.常温常压下,1.6g O2和O3混合气体中质子总数为0.8 NA |
| C.一定条件下,2mol SO2和 1mol O2发生反应,转移的电子总数一定是2NA |
| D.1L 0.1mol·L-1的葡萄糖溶液中分子总数为0.1 NA |