已知:①1 mol H2分子中化学键断裂时需要吸收 436kJ 的能量
②1 mol Cl2分子中化学键断裂时需要吸收 243kJ 的能量
③由H原子和Cl原子形成1mol HCl分子时释放 431kJ 的能量,则下列叙述正确的是
| A.氢气和氯气反应生成氯化氢气体的热化学方程式是 H2 (g) + Cl2 (g) =2HCl(g) |
| B.氢气和氯气反应生成 2 mol 氯化氢气体,反应的△H ="+183" kJ·mol-1 |
| C.氢气和氯气反应生成 2 mol 氯化氢气体,反应的△H =-183 kJ·mol-1 |
| D.氢气和氯气反应生成 1 mol 氯化氢气体,反应的△H =-183 kJ·mol-1 |
具有下列特征的原子一定是非金属元素的是
| A.最外层电子数大于4 |
| B.具有负化合价 |
| C.最高价氧化物对应水化物是酸 |
| D.具有可变化合价 |
X、Y、Z三种短周期元素,X元素的原子最外层只有一个电子,Y元素的原子M电子层的电子数为K、L上电子总数的一半,Z元素的原子L层电子数比Y原子L层电子数少2个,由这三种元素组成的化合物的化学式可能是
| A.X3YZ4 | B.X2YZ3 |
| C.XYZ2 | D.X2YZ4 |
某元素原子的最外层电子数是次外层的电子数的n倍(n为大于1的自然数),则该原子核内的质子数是
| A.2n | B.n+2 |
| C.2n+10 | D.2n+2 |
带有2个单位正电荷微粒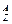 X2+,它的质量数A等于137,中子数是81,则该粒子核外电子数是
X2+,它的质量数A等于137,中子数是81,则该粒子核外电子数是
| A.56 | B.54 | C.58 | D.137 |
下列原子结构示意图中,正确的是