反应4NH3(g)+5O2(g)=4NO(g)+6H2O(g)在2升密闭容器中进行1分钟后,NH3减少了0.12 mol,则平均每秒钟浓度变化正确的是
| A.H2O:0.002 mol·L-1 | B.NO:0.001 mol·L-1 |
| C.NH3: 0.002 mol·L-1 | D.O2:0.0025 mol·L-1 |
化学与生活、社会密切相关,下列说法错误的是
| A.玻璃属于无机非金属材料 | B.煤的气化属于物理变化 |
| C.雾霾与汽车尾气的排放有关 | D.甲醛的水溶液可以用来浸泡标本 |
锌-溴蓄电池的充、放电的电池总反应为Zn+Br2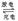 Zn2++2Br-,下列各反应:①Zn-2e-=Zn2+;②Br2+2e-=2Br-;③2Br--2e-=Br2;④Zn2++2e-=Zn,其中充电的阳极和放电的负极的反应分别是
Zn2++2Br-,下列各反应:①Zn-2e-=Zn2+;②Br2+2e-=2Br-;③2Br--2e-=Br2;④Zn2++2e-=Zn,其中充电的阳极和放电的负极的反应分别是
| A.①② | B.③② | C.④② | D.③① |
已知某金属元素R的+1价阳离子最外层有2个电子,该阳离子有6个电子层下列推断正确的是
| A.R元素位于第6周期,ⅢB族 |
| B.R(OH)3与Al(OH)3一样是两性氢氧化物 |
| C.R单质还原性比铝强 |
| D.离子半径:R3+>R+ |
有A、B、C三种短周期元素,已知A元素的原子最外层电子数等于其电子层数,B元素的原子最外层电子数是其电子层数的2倍,C元素的原子最外层电子数是其电子层数的3倍。由三种元素组成的化合物的化学式不可能是
A.A3BC4 B.A2(BC4)3C.A2BC3D.ABC4
几种短周期元素的原子半径及主要化合价见下表:
| 元素代号 |
L |
M |
Q |
R |
T |
| 原子半径/nm |
0.160 |
0.143 |
0.102 |
0.089 |
0.074 |
| 主要化合价 |
+2 |
+3 |
+6、-2 |
+2 |
-2 |
下列叙述正确的是
A.L、R的单质与稀盐酸反应速率L<R
B.M与R性质相似
C.Q、T两元素的氢化物沸点:T的氢化物低于Q的氢化物
D.L、M、Q形成的简单离子半径由大到小顺序是L>M>Q