已知Fe(s)+H2SO4(aq)=FeSO4(aq)+H2(g) ΔH<0,则下列关于该反应的叙述不正确的是
| A.化学键的断裂和形成是化学反应中能量变化的主要原因 |
| B.上述热化学方程式中的ΔH的值与反应物的用量有关 |
| C.该反应的化学能可以转化为电能 |
| D.此反应构成的原电池中,正极可以是碳棒、铜或锌 |
高温下,某反应达平衡,平衡常数K=。恒容时,温度升高,H2浓度减小。下列说法正确的是()
| A.该反应化学方程式为CO + H2O催化剂高温 CO2+ H2 |
| B.升高温度,逆反应速率减小 |
| C.该反应的焓变为正值 |
| D.恒温恒容下,增大压强,H2浓度一定减小 |
测得某反应A+B 2C在不同温度下的平衡常数:
2C在不同温度下的平衡常数:
| 温度 |
500C |
800C |
| K |
100 |
400 |
又测得温度t时,反应2C A+B的平衡常数为0.05,可推知t的范围是()
A+B的平衡常数为0.05,可推知t的范围是()
A. t<500C B. t>800C C. 500C<t<800C D. 无法确定
一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:下列描述正确的是()
A.反应的化学方程式为:X(g)+ Y(g) Z(g) Z(g) |
| B.反应开始到10s,X的物质的量浓度减少了0.79mol/L |
| C.反应开始到10s时,Y的转化率为79.0% |
| D.反应开始到10s,用Z表示的反应速率为0.158mol/(L·s) |
下图装置中,U型管内为红墨水,a.b试管内分别盛有食盐水和氯化铵溶液(溶液呈弱酸性),各加入生铁块,放置一段时间。下列有关描述错误的是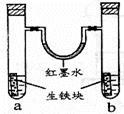
| A.生铁块中的碳是原电池的正极 |
| B.红墨水柱两边的液面变为左低右高 |
| C.两试管中相同的电极反应式是:Fe-2e-=Fe2+ |
| D.a试管中发生了吸氧腐蚀,b试管中发生了析氢腐蚀 |
下列说法不正确的是()
| A.铸铁输油管道应埋在干燥致密不透气的土壤中 |
| B.在空气中,金属铝表面能迅速被氧化形成保护膜,因此铝不容易被腐蚀 |
| C.钢铁发生电化学腐蚀时,负极发生的反应是2H2O+O2+4e-= 4OH- |
| D.白铁(镀Zn铁)表面有划损时,也能阻止铁被氧化 |