下列有关氨的说法正确的是
| A.氨是弱电解质,铵盐是强电解质 |
| B.液氨是纯净物,氨水是混合物 |
| C.氨气遇浓盐酸、浓硫酸、浓硝酸都能产生白烟 |
| D.氨气易液化,所以可用来做喷泉实验 |
下列叙述正确的是
| A.沼气和水煤气都是可再生能源 |
| B.石油裂解和油脂皂化都有高分子生成小分子的过程 |
| C.不能用植物油萃取溴水中的溴 |
| D.可以用加热使蛋白质变性的方法分离提纯蛋白质 |
化学与社会、生产、生活密切相关。下列说法正确的是
| A.可以用物理方法或化学方法从海水中提取所需物质 |
| B.用激光笔分别照射盛有牛奶、食盐水的玻璃杯,都有光亮的通路 |
| C.神舟10号飞船所用太阳能电池板可将光能转换为电能,所用转换材料是二氧化硅 |
| D.氯气溶于水生成次氯酸有强氧化性,可以起到除去水中杂质和杀菌消毒作用 |
常温下,将Cl2缓慢通入一定量的水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol·L-1的氢氧化钠溶液,整个过程中pH变化如图所示,下列有关叙述正确的是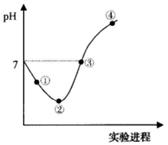
| A.②点之前所发生反应的离子方程式为Cl2+H2O=2H++Cl-+ClO﹣ |
| B.③点所示溶液中:c(Na+)= c(HClO)+2c(ClO-) |
| C.实验进程中溶液的pH可以用pH试纸测得 |
| D.曲线的起始点水的电离程度最大 |
下列有关说法正确的是
A.对于反应2SO2(g)+O2(g)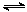 2SO3(g),压缩气体体积使压强增大(其他条件不变),则SO2的转化率增大,平衡常数K也增大 2SO3(g),压缩气体体积使压强增大(其他条件不变),则SO2的转化率增大,平衡常数K也增大 |
| B.电解法精炼铜时,精铜作阳极,粗铜作阴极 |
| C.在硫酸钡悬浊液中加入足量饱和Na2CO3溶液处理,向所得沉淀中加入盐酸有气体产生,说明Ksp(BaSO4)>Ksp(BaCO3) |
D.CH3COOH溶液加水稀释后,电离程度增大,溶液中 的值不变 的值不变 |
下列实验的现象与对应的结论均正确的是
| 选项 |
操作 |
现象 |
结论 |
| A |
向溶液X中滴加NaOH稀溶液,将湿润的红色石蕊试纸置于试管口 |
试纸不变蓝 |
溶液X中无NH |
| B |
将少量的溴水滴入FeCl2、NaI的混合溶液中,再滴加CCl4,振荡、静置,向上层溶液中滴加KSCN溶液 |
上层溶液不变红, 下层溶液紫红色 |
氧化性:Br2>Fe3+>I2 |
| C |
将水蒸气通过灼热的铁粉 |
粉末变红 |
铁与水在高温下发生反应 |
| D |
向漂白粉上加入较浓的盐酸,将湿润淀粉碘化钾试纸置于试管口 |
产生气泡,试纸未变蓝 |
漂白粉已经失效 |