(双选)短周期元素W、X、Y、Z在元素周期表中的相对位置如下图所示,其中Y所处的周期序数与族序数相等。W最外层电子数是内层电子数的3倍。下列说法正确的是
| |
|
|
… |
W |
| X |
|
Y |
… |
Z |
A.X、Y、Z、W的原子半径依次减小
B.W与X形成的化合物中只含离子键
C.W的气态氢化物的稳定性小于Z的气态氢化物的稳定性
D.W与Y形成的化合物可分别与NaOH溶液和盐酸反应
物质的鉴别有多种方法。下列能达到鉴别目的的是( )
①用水鉴别苯、乙醇、溴苯
②用相互滴加的方法鉴别Ca(OH)2和NaHCO3溶液
③点燃鉴别甲烷和乙炔
| A.①② | B.①③ | C.②③ | D.①②③ |
下列检验阿司匹林有效成分中所含官能团的方案正确的是(双选)( )
A.阿司匹林清液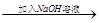 酯基水解 酯基水解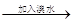 检验酯基 检验酯基 |
B.阿司匹林清液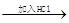 酯基水解 酯基水解 检验酯基 检验酯基 |
C.阿司匹林清液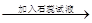 检验羧基 检验羧基 |
D.阿司匹林清液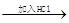 酯基水解 酯基水解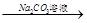 振荡 振荡 检验酯基 检验酯基 |
某有机物的结构简式为 ,该物质1 mol与足量NaOH溶液充分反应,消耗NaOH的物质的量为( )
,该物质1 mol与足量NaOH溶液充分反应,消耗NaOH的物质的量为( )
| A.5 mol | B.4 mol |
| C.3 mol | D.2 mol |
阿司匹林药效释放较快,科学家将它连接在高分子载体上制成缓释长效阿司匹林,其中一种药物结构简式如下: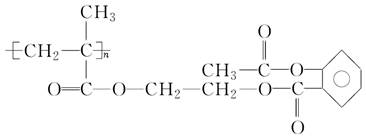
该物质1 mol与足量NaOH溶液反应,消耗NaOH的物质的量为( )
| A.3 mol | B.4 mol |
| C.3n mol | D.4n mol |
人剧烈运动,骨骼肌组织会供氧不足,导致葡萄糖无氧氧化,产生大量酸性物质(分子式为C3H6O3),如果该物质过度堆积于腿部,会引起肌肉酸痛。体现该物质酸性的基团是( )
| A.羟基 | B.甲基 |
| C.乙基 | D.羧基 |