碱性硼化钒(VB2)—空气电池工作时反应为:4VB2 + 11O2 = 4B2O3 + 2V2O5。用该电池为电源,选用惰性电极电解硫酸铜溶液,实验装置如图所示。当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是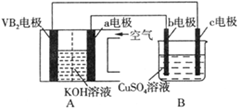
| A.VB2电极发生的电极反应为:2VB2 + 11H2O - 22e- = V2O5 + 2B2O3 + 22H+ |
| B.外电路中电子由c电极流向VB2电极 |
| C.电解过程中,b电极表面先有红色物质析出,然后有气泡产生 |
| D.若B装置内的液体体积为200 mL,则CuSO4溶液的物质的量浓度为0.05 mol/L |
在下列给定条件的溶液中,一定能大量共存的离子组是( )
| A.无色溶液:Na+、H+、Cl-、ClO- |
| B.能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3- |
| C.FeCl2溶液:K+、Na+、SO42-、OH- |
D. ="0.1" mol/L的溶液:Na+、K+、SiO32-、NO3- ="0.1" mol/L的溶液:Na+、K+、SiO32-、NO3- |
25℃时,水的电离达到平衡:H2O H++OH-;ΔH>0,下列叙述正确的是
H++OH-;ΔH>0,下列叙述正确的是
| A.向水中加入稀氨水,平衡逆向移动,c(OH—)降低 |
| B.向水中加入少量固体硫酸氢钠(温度变化忽略不计),c(H+)增大,Kw不变 |
| C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| D.将水加热,Kw增大,pH不变 |
用已知浓度的盐酸滴定未知浓度的NaOH溶液,选用酚酞作指示剂,下列操作会导致测定结果偏低的是()
| A.酸式滴定管用蒸馏水洗后未用标准液润洗就装标准液滴定 |
| B.锥形瓶未用待测液润洗 |
| C.读取标准液读数时,滴前仰视,滴定到终点后俯视 |
| D.滴定前酸式滴定管尖嘴处有气泡未排除,滴定后气泡消失 |
将0.1 mol/L CH3COOH溶液加水稀释或加入少量CH3COONa晶体时,都会引起( )
| A.溶液的pH增大 |
| B.CH3COOH电离度增大 |
| C.溶液的导电能力减弱 |
| D.溶液中c(OH-)减小 |
下列关于纯净物、混合物、强电解质、弱电解质、非电解质的组合正确的是()
| 纯净物 |
混合物 |
强电解质 |
弱电解质 |
非电解质 |
|
| A |
大理石 |
玻璃 |
氯化钾 |
高氯酸 |
干冰 |
| B |
盐酸 |
水煤气 |
硫酸 |
醋酸 |
氯气 |
| C |
明矾 |
水泥 |
苛性钠 |
亚硫酸 |
熟石灰 |
| D |
冰醋酸 |
漂白粉 |
BaSO4 |
氟化氢 |
氨气 |