向含有Fe2+、Al3+、NH4+、Na+、K+的溶液中加入过量的Na2O2固体,微热溶液使其充分反应,再通入过量的HCl气体,则反应后溶液中离子浓度大量减小的是
| A.Na+和K+ | B.Al3+和Na+ |
| C.Fe2+和NH4+ | D.Fe2+和K+ |
下列化学变化中,需加入氧化剂才能实现的是
| A.C→CO2 | B.CO2→CO | C.CuO→Cu | D.H2SO4→BaSO4 |
下列说法错误的是:
| A.钠在空气燃烧时先熔化,再燃烧,最后所得的产物是Na2O2 |
| B.铝因在空气中形成了一薄层致密的氧化膜,保护内层金属,故铝不需特殊保护 |
| C.铝制品在生活中非常普通,是因为铝非常不活泼 |
| D.铁因在潮湿的空气中形成的氧化物疏松,不能保护内层金属 |
下列实验操作正确的是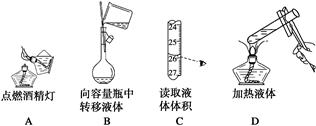
下列有关阿佛加德罗常数(NA)的说法错误的是
A.32克O2所含的原子数目为NAB.0.5 molH2O含有的原子数目为1.5 NA
C.1 molH2O含有的H2O分子数目为NA D.0.5 mol氯气含有的分子数目为0.5 NA
Na2CO3俗名纯碱,下面是对纯碱采用不同分类法的分类,不正确的是
| A.Na2CO3是碱 | B.Na2CO3是盐 |
| C.Na2CO3是钠盐 | D.Na2CO3是碳酸盐 |