有200mL氯化镁和氯化铝的混合溶液,其中c(Mg2+)为0.2mol・L-1,c(Cl-)为1.3mol・L-1。要使Mg2+全部转化为沉淀分离出来,至少需加4mol・L-1NaOH溶液的体积为
| A.40mL | B.72mL | C.80mL | D.128mL |
在一体积可变的密闭容器中,加入一定量的X、Y,发生反应 。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
 气体体积/L 气体体积/Lc(Y)/mol·L-1 温度/℃ |
1 |
2 |
4 |
| 100 |
1.00 |
0.75 |
0.53 |
| 200 |
1.20 |
0.90 |
0.63 |
| 300 |
1.30 |
1.00 |
0.70 |
下列说法正确的是()
A.m>n B.温度不变,压强增大,Y的质量分数减少
C.Q<0 D.体积不变,温度升高,平衡向逆反应方向移动
已知一种c(H+)=1×10-3 mol/L的酸和一种c(OH-)=1×10-3 mol/L的碱溶液等体积混合后溶液呈酸性,其原因可能是()
| A.浓的强酸和稀的强碱溶液反应 | B.浓的弱酸和稀的强碱溶液反应 |
| C.等浓度的强酸和弱碱溶液反应 | D.生成了一种强酸弱碱盐 |
已知乙酸(HA)的酸性比甲酸(HB)弱,在物质的量浓度均为0.1 mol/L的NaA和NaB混合溶液中,下列排序正确的是()
A.c(OH-)>c(HA)>c(HB)>c(H+) B.c(OH-)>c(A-)>c(B-)>c(H+)
C.c(OH-)>c(B-)>c(A-)>c(H+) D.c(OH-)>c(HB)>c(HA)>c(H+)
pH相同的醋酸溶液和盐酸,分别用蒸馏水稀释至原体积的m倍和n倍,稀释后两溶液pH仍相同,则m和n的关系是()
| A.m=n | B.m>n | C.m<n | D.无法判断 |
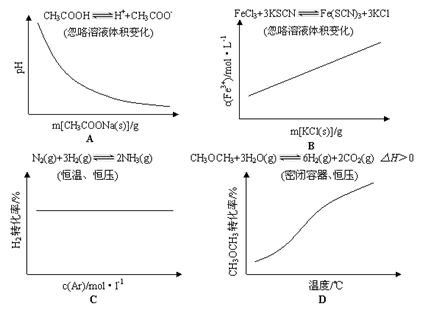
各可逆反应达到平衡后,改变反应条件,其变化趋势正确的是()