将一定量的锌与100mL 18.5mol/L浓硫酸充分反应后,锌完全溶解,同时生成气体A为33.6L(标准状况).将反应后的溶液稀释至1L,测得溶液的c(H+)=0.1mol·L-1,则下列叙述中错误的是
| A.气体A为SO2和H2的混合物 | B.气体A中SO2和H2的体积比为4:1 |
| C.反应中共消耗Zn 97.5g | D.反应中共转移3mol电子 |
下列每组物质发生状态变化所克服的微粒间的相互作用属同种类型是
| A.食盐和蔗糖的熔化 | B.白磷和硫的熔化 |
| C.氯化铵固体和干冰受热后的气化 | D.氧化镁和金属镁的熔化 |
“嫦娥一号”卫星上使用的一种高能电池——银锌蓄电池,其电池的电极反应式为:
Zn-2e-+2OH―=ZnO+H2O,Ag2O+H2O+2e-=2Ag+2OH-。据此判断氧化银是
| A.负极,被氧化 | B.正极,被还原 | C.负极,被还原 | D.正极,被氧化 |
雷雨天闪电时空气中有臭氧(O3)生成。下列说法中正确的是
| A.相同质量的O2和O3原子个数比为2:3 |
| B.O2和O3化学性质完全相同 |
| C.在相同温度与压强下,等体积的O2和O3含有相同的分子数 |
| D.O2和O3的相互转化是物理变化 |
对于可逆反应2SO2+O2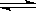 2SO3,在混合气体中充入一定量的18O2,足够长的时间后,18O原子
2SO3,在混合气体中充入一定量的18O2,足够长的时间后,18O原子
| A.只存在于O2中 | B.只存在于O2和SO3中 |
| C.只存在于O2和SO2中 | D.存在于O2、SO2和SO3中 |
下列关于化学理论学习和研究的说法错误的是
| A.化学键的变化不一定会引起化学反应的变化 |
| B.外界条件改变一定会引起化学反应的快慢变化 |
| C.化学模型的建立有助于解释一些化学现象 |
| D.化学基本原理的应用是建立在有一定条件的基础上的 |