高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:
下列叙述不正确的是
| A.放电时负极反应为:Zn - 2e—+ 2OH— ="=" Zn(OH)2 |
| B.充电时阳极反应为:Fe(OH)3 -3e— + 5OH— ="=" FeO42— + 4H2O |
| C.放电时每转移3moL电子,正极有1 mol K2FeO4被氧化 |
| D.放电时正极附近溶液的碱性增强 |
已知短周期元素的离子:aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是
| A.原子半径A>B>D>C | B.原子序数d>c>b>a |
| C.离子半径C>D>B>A | D.单质的还原性A>B>D>C |
下列说法正确的是
①水分子之间存在氢键,所以水受热不易分解
②共价化合物一定含共价键,也可能含离子键
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
⑥熔化状态下能导电的物质不一定是离子化合物
⑦有单质生成的反应一定是氧化还原反应
⑧碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物
| A.③⑤⑥⑦⑧ | B.②③④⑥⑦ |
| C.③⑥⑧ | D.①③④⑥ |
下列化学表达方式不正确的是
| A.中子数为20的氯原子:37Cl |
B.Cl-的结构示意图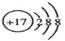 |
C.氢氧根离子的电子式: |
| D.HClO的结构式 H-Cl-O |
重水(D2O)是重要的核工业原料,下列说法错误的是
A.氘(D)原子核外有1个电子
B.1H与D互称同位素
C.H2O与D2O互称同素异形体
D.1H218O与D216O的相对分子质量相同
某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是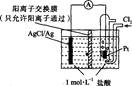
| A.正极反应为AgCl+e-═Ag+Cl- |
| B.放电时,交换膜右侧溶液中有大量白色沉淀生成 |
| C.若用NaCl溶液代替盐酸,则电池总反应随之改变 |
| D.当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子 |