下列各项表述与示意图一致的是
| A.图①中a、b曲线分别表示反应CH2=CH2(g)+H2(g) →CH3CH3(g) +ΔQ ,0<ΔQ;使用和未使用催化剂时,反应过程中的能量变化 |
| B.图②表示25 ℃时,用0.01 mol·L-1盐酸滴定一定体积的0.01 mol·L-1 NaOH溶液,溶液的pH随加入酸体积的变化 |
C.图③表示CH4(g)+H2O(g) CO(g)+3H2(g) +ΔQ ,反应CH4的转化率与温度、压强的关系,且p1>p2、0<ΔQ CO(g)+3H2(g) +ΔQ ,反应CH4的转化率与温度、压强的关系,且p1>p2、0<ΔQ |
D.图④中曲线表示反应2SO2(g)+O2(g)  2SO3(g) +ΔQ ,0<ΔQ;正、逆反应的平衡常数K随温度的变化 2SO3(g) +ΔQ ,0<ΔQ;正、逆反应的平衡常数K随温度的变化 |
下列有关电化学装置的说法正确的是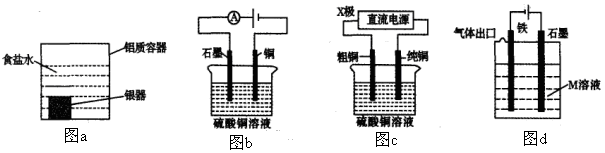
| A.利用图a装置处理银器表面的黑斑Ag2S,银器表面发生的反应为Ag2S+2e-=2Ag+S2- |
| B.图b电解一段时间,铜电极溶解,石墨电极上有亮红色物质析出 |
| C.图c中的X极若为负极,则该装置可实现粗铜的精炼 |
| D.图d中若M是海水,该装置是通过“牺牲阳极的阴极保护法”使铁不被腐蚀 |
下列说法错误的是
| A.除去MgCl2溶液中少量的FeCl3,可选用MgCO3 |
| B.稀硫酸中加入Zn粉,随着反应的进行,溶液中水的电离程度逐渐增大 |
| C.能溶解氧化铝的溶液中可能大量存在:HCO3-、SO42-、NO3-、Na+ |
| D.等物质的量浓度的(NH4)2SO4溶液和(NH4)2CO3溶液中NH4+浓度前者大于后者 |
在密闭容器中充入一定量的NO2,发生反应2NO2(g) N2O4(g)△H=-57kJ/mol,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如下图所示。下列说法正确的是
N2O4(g)△H=-57kJ/mol,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如下图所示。下列说法正确的是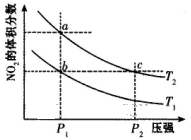
| A.a、c两点的反应速率:a>c |
| B.a、b两点的转化率:a<b |
| C.a、c两点气体的颜色:a深,c浅 |
| D.由a点到b点,可以用加热的方法 |
下列事实能说明亚硫酸的酸性强于碳酸的是
| A.饱和亚硫酸溶液的pH小于饱和碳酸溶液的pH |
| B.亚硫酸能使酸性高锰酸钾溶液褪色,而碳酸不能 |
| C.同温下,等浓度的亚硫酸氢钠和碳酸氢钠溶液,碳酸氢钠溶液的碱性强 |
| D.将过量二氧化硫气体通入碳酸氢钠溶液中,逸出的气体能使澄清石灰水变浑浊 |
下列有关实验操作、现象和解释或结论都正确的是
| 选项 |
实验操作 |
现象 |
解释或结论 |
| A |
常温下铜片插入浓硫酸中 |
无明显现象 |
常温下铜浓硫酸钝化 |
| B |
将水蒸气通过灼热的铁粉 |
铁粉变成红棕色粉末 |
铁粉与水在高温下发生反应 |
| C |
将SO2通入滴有酚酞的NaOH溶液中 |
溶液红色褪去 |
SO2具有漂白性 |
| D |
向某溶液中先加入稀盐酸,后加入氯化钡溶液 |
先加稀盐酸无明显现象,后加氯化钡溶液有白色沉淀生成 |
溶液中存在SO42- |