在25℃时,某稀溶液中由水电离产生的c(OH-)水=10-11mol/L。下列有关该溶液的叙述正确的是
| A.该溶液一定呈酸性 |
| B.该溶液中的c(H+)肯定等于10-3mol/L |
| C.该溶液的pH可能为3,可能为11 |
| D.该溶液一定呈碱性 |
一定温度下,某密闭容器中发生反应:2HI(g) H2(g)+I2(g)△H>0,若15s内c(HI)由0.1 mol·L-1降到0.07 mol·L-1,则下列说法正确的是
H2(g)+I2(g)△H>0,若15s内c(HI)由0.1 mol·L-1降到0.07 mol·L-1,则下列说法正确的是
| A.15s内用H2表示的平均反应速率为v(H2)="0.002" mol·L-1·s-1 |
| B.升高温度平衡逆向移动 |
| C.c(HI)由0.07 mol·L-1降到0.05 mol·L-1所需时间为10s |
| D.减小反应体系的体积,化学反应速率加快 |
在密闭容器中存在如下反应:A (g)+3B(g) 2C(g);△H<0,某研究小组研究了只改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:
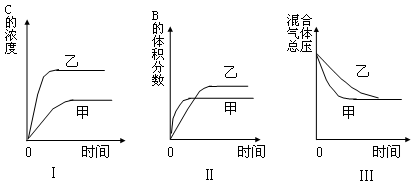
下列判断一定错误的是
| A.图Ⅰ研究的是压强对反应的影响,且乙的压强较高 |
| B.图Ⅱ研究的是压强对反应的影响,且甲的压强较高 |
| C.图Ⅱ研究的是温度对反应的影响,且甲的温度较高 |
| D.图Ⅲ研究的是不同催化剂对反应的影响,且甲使用催化剂的效率较高 |
有关溶液中的反应3KSCN+FeCl3 Fe(SCN)3+3KCl的研究,下列说法不正确的是
Fe(SCN)3+3KCl的研究,下列说法不正确的是
| A.向平衡体系中加入少量KCl固体,溶液红色变浅 |
| B.加入少量FeCl3固体,溶液红色加深 |
| C.给体系加压,溶液红色没有明显变化 |
| D.Fe(SCN)3属于盐类,是一种弱电解质 |
某温度下在密闭容器中发生如下反应:2SO2(g)+O2(g) 2SO3(g),若开始时只充入2 molSO3,达到平衡时,混合气体的压强比起始时增大了10%;若开始时只充入了2 mol SO2和1 molO2的混合气体,达到平衡时SO2的转化率为:
2SO3(g),若开始时只充入2 molSO3,达到平衡时,混合气体的压强比起始时增大了10%;若开始时只充入了2 mol SO2和1 molO2的混合气体,达到平衡时SO2的转化率为:
| A.10% | B.60% | C.80% | D.90% |
关于石油的说法中,不正确的是
| A.石油主要含烃类物质,这些烃类物质随着烃分子含有的碳原子数的增加沸点升高 |
| B.常压分馏得到的汽油是混合物,没有固定的沸点,但石油气为纯净的丙烷 |
| C.石油分馏不是化学变化,但裂化是化学变化 |
| D.裂化的目的是得到轻质油,裂解的目的是得到乙烯、丙烯等化工原料 |