以化学的视角来认识青奥会。
(1)图A中金可以压制成金币,说明金具有良好的 性。某纪念币是由合金铸造的,其熔点比成分金属熔点 (填“高”或“低”)。
(2)为减少传统燃油汽车的尾气污染,南京近期投入了一批液化天然气公交车和电动公交车。
①写出天然气燃烧的化学方程式 。电动公交车上的电池是将化学能转化成 能的装置。
②电动车一般使用铅酸蓄电池。某铅酸蓄电池使用的酸溶液是质量分数为20%的稀硫酸。若用50 g质量分数为98%的浓硫酸配制该稀硫酸时,需要加水 mL(水的密度为1g/mL);在实验室用浓硫酸配制稀硫酸的主要步骤有:计算、 、混匀、装瓶并贴上标签;若用量筒量取浓硫酸时俯视读数,所配溶液中溶质的质量分数 20%(填“大于”、“小于”或“等于”)。
在宏观、微观和符号之间建立联系是化学学科的特点。
(1)叶绿素(C55H72MgN4O5)是植物进行光合作用的重要物质,该物质由种元素组成
(2)氧气、铁和氯化钠三种物质中,由离子构成的是。(填化学用语)
(3)从微观变化角度,“CO燃烧”的微观示意图,如图所示。
写出上述过程的化学方程式
人体缺乏维生素C(简写“Vc”)会患坏血病。下图所示为某种“维生素C”说明书的一部分,请回答:
(1)“Vc”属于________________化合物(填“无机”或“有机”);
(2)“Vc”中C、H、O三种元素的质量比是________________;
(3)若正常成人每天对“Vc”的最低需要量为60mg:
①当这些“Vc”完全来自右图的“维生素C”时,则每次服用“维
生素C”至少_______片;
根据下列装置图,回答有关问题:
(1)写出图中标号仪器的名称:①;
(2)实验室以高锰酸钾为原料制氧气的化学方程式是;作为发生装置,装置A需要改进的地方是。
(3)实验室制二氧化碳的药品为和,为了得到纯净的二氧化碳气体,要除去二氧化碳气体中的氯化氢可选胜出下列试剂中的(选填字母)。
A NaOH溶液 B H2SO4溶液 C NaHCO3溶液D Na2CO3溶液
(4)已知实验室制取氯气的反应原理是:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,选择的发生装
MnCl2+Cl2↑+2H2O,选择的发生装
置是,若用下图所示装置测量生成氯气的体积,装置接口的连接顺序为a →→→d。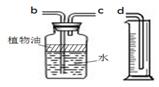
某经济开发区将钛冶炼厂与氯碱厂、甲醇厂组成了一个产业链(如图所示),大大提高了资源利用率,减少了环境污染.请填写:
氯碱厂用电解饱和食盐水的方法制取烧碱,同时得到氯气和氢气.写出其化学方程式:
(2)钛冶炼厂氯化车间的氯化过程发生如下反应:2FeTiO3+6C+7Cl2=2X+2TiCl4+6CO,则X的化学式为
(3)试写出TiCl4与Mg反应生成金属Ti的化学方程式 ,上述反应需在氩气环境中进行,理由是
(4)同温同压下,任何气体之间的体积比就是它们的分子数之比.在一定条件下用H2和CO化合生成甲醇(化学方程式是2H2+CO═CH3OH),则合成甲醇时,H2和CO两种气体的体积比应为
如图为NaCl、KNO3的溶解度曲线,回答下列问题:
(1)20℃时,KNO3的溶解度是 g。
(2)某实验小组进行以下实验:
10 g水 X
X Y
Y  Z
Z
X、Y、Z中为饱和溶液的是 。
(3)把NaCl的不饱和溶液变为饱和溶液,下列方法中一定可行的是(填序号)
A.降低温度 B.加入NaCl固体 C.蒸发溶剂
(4)提纯KNO3中混有少量的NaCl 可采用方法