下列溶液中粒子的物质的量浓度关系正确的是
| A.0.1mol/LNaHCO3溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-) |
| B.20mL0.1mol/LCH3COONa溶液与10mL0.1mol/LHCl溶液混合后呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) |
| C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
| D.0.1mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH) |
下列说法正确的是()
| A.可用使铁钝化的方法来减缓铁的腐蚀 |
| B.除去CO气体中的少量氧气可让气体通过加热的铜网 |
| C.不论将铝箔加热到什么样的温度均是只熔化而不滴落下来 |
| D.等质量的铝与盐酸或氢氧化钠溶液反应时产生的氢气体积一定相等 |
2010年国家又再次提出奶粉中三聚氰胺的添加标准,食用三聚氰胺会使受污染奶粉的婴幼儿产生肾结石病症。经调查是一些不法商人用三聚氰胺作奶粉添加剂,以提升奶粉检测中的蛋白质含量指标和增加产品的含水量。以下有关三聚氰胺(结构简式如图)的说法错误的是()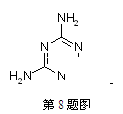
| A.该分子为非极性分子 |
| B.该物质的水溶液显弱碱性,能与盐酸反应. |
| C.该物质有毒,不能作食品添加剂 |
| D.三聚氰胺为有刺激性气味的深黄色物质 |
右图为电解饱和食盐水的简易装置,其中蛋壳内壁的半透膜已替换成阳离子交换膜,蛋壳内外均装有饱和食盐水,铁丝缠在蛋壳上,碳棒在蛋壳内,下列有关说法中正确的是()
| A.电解一段时间后,往蛋壳内的溶液中滴加几滴酚酞,呈红色 |
| B.蛋壳表面缠绕的铁丝发生氧化反应 |
| C.铁丝表面生成的气体能使湿润的淀粉碘化钾试纸变蓝 |
D.该装置可阻 止生成的氯气与氢气、氢氧化钠溶液接触 止生成的氯气与氢气、氢氧化钠溶液接触 |
某化学兴趣小组对北京奥运会金牌的成分提出猜想:甲认为金牌属纯金制品;乙认为金牌属纯银镀金制品;丙认为金牌属纯铜镀金制品。为了验证他们的猜想,可选用的试剂是()
| A.硫酸铜溶液 | B.盐酸 |
| C.稀硝酸 | D.硝酸银溶液 |
一定条件下,对于可逆反应X(g)+3Y(g)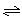 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.08 mol/L,则下列判断正确的是
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.08 mol/L,则下列判断正确的是
| A.c1∶c2=3∶1 | B.平衡时,Y和Z的生成速率之比为2∶3 |
| C.X、Y的转化率相等 | D.c1的取值范围为0.04 mol/L<c1<0.14 mol/L |