以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,其工作原理如图所示。下列说法正确的是
| A.电池放电时Na+从b极区移向a极区 |
| B.该电池的负极反应为:BH4-+8OH--8e-===BO2-+6H2O |
| C.电极a采用MnO2,MnO2既作电极材料又有催化作用 |
| D.每消耗3 mol H2O2,转移的电子为3 mol |
下列有关判断正确的是
| A.由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:Cu-2e-=Cu2+ |
| B.由Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3e-+3OH-=Al(OH)3 |
| C.由Al、Cu、浓硝酸组成原电池,其负极反应式为:Cu-2e-=Cu2+ |
| D.用原电池和电解池装置都能实现2HCl + Cu=CuCl2 + H2↑ 反应 |
在铁的电化学腐蚀中,发生还原反应的那个电极上进行的电极反应是( )
| A.2H2O+O2+4e-===4OH- |
| B.2H++2e-===H2 |
| C.4OH--4e-===2H2O+O2 |
| D.Fe-2e-===Fe2+ |
已知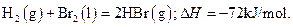 蒸发1mol Br2(l)需要吸收的能量为30kJ,其它相关数据如下表:
蒸发1mol Br2(l)需要吸收的能量为30kJ,其它相关数据如下表:
| H2(g) |
Br2(g) |
HBr(g) |
|
1mol分子中的化学键断裂 时需要吸收的能量/KJ 时需要吸收的能量/KJ |
436 |
a |
369 |
则表中a为( )
A.404 B.260 C.230D.200
下列说法或表示方法中正确的是()
| A.等质量的硫蒸气和硫固体分别完全燃烧,反应的热效应ΔH1>ΔH2 |
B.由C(石墨)→C(金刚石);ΔH="+1.9KJ/mol" , 可知1 mol石墨的总键能比1 mol金刚石的总键能大1.9 kJ,即金刚石比石墨稳定 可知1 mol石墨的总键能比1 mol金刚石的总键能大1.9 kJ,即金刚石比石墨稳定 |
C.在101KPa时,2gH2完全燃烧生成液态水,放出285.8 KJ热量,氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l);ΔH=+285.8KJ/mol KJ热量,氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l);ΔH=+285.8KJ/mol |
| D.在稀溶液中:H+( aq )+OH-( aq)=H2O(l);ΔH="-57.3KJ/mol" ,若将0.5 mol浓H2SO4溶液与含1 molNaOH的溶液混合,放出的热量大于57.3KJ |
有两只串联的电解池(Pt为电极),甲池盛有足量的CuSO4溶液,乙池盛有足量的某硝酸盐的稀溶液。电解时当甲池电极析出6.4gCu时,乙池电极析出21.6g 金属,则乙池的溶质可能是()
金属,则乙池的溶质可能是()
| A.NaNO3 | B.Cu(NO3)2 | C.Al(NO3)3 | D.AgNO3 |