下列分子中,所有原子的最外层均为8电子结构的是()
| A.BeCl2 | B.HClO | C.PCl5 | D.P4 |
下列离子方程式书写正确的是()
A.溴乙烷与6mol/L 的氢氧化钠水溶液共热: 的氢氧化钠水溶液共热:C2H5Br+OH- 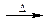 CH2=CH2↑+Br-+H2O CH2=CH2↑+Br-+H2O |
| B.等物质的量浓度、等体积的Ca(HCO3)2溶液与氢氧化钠溶液相混合: Ca2++2HCO3-+2OH-  CaCO3↓+CO32-+2H2O CaCO3↓+CO32-+2H2O |
| C.在含有等物质的量的Fe(NO3)2和KI组成的混合溶液中滴入1~2滴盐酸: 3Fe2++4H++NO3-  3Fe3++NO↑+2H2O 3Fe3++NO↑+2H2O |
| D.在H2O2中加入酸性高锰酸钾溶液: |
2MnO4-+6H++5H2O2 2Mn2++5O2↑+8H2O
2Mn2++5O2↑+8H2O
在下列给定条件的溶液中,一定能大量共存的离子组是()
| A.无色溶液:Ca2+、H+、Cl-、HSO3- |
| B.能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3- |
| C.FeCl2溶液:K+、Na+、SO42-、AlO2- |
D.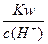 =01mol/L的溶液:Na+、K+、SiO32-、NO3- =01mol/L的溶液:Na+、K+、SiO32-、NO3- |
下列有关实验操作的说法正确的是()
| A.可用25mL碱式滴定管量取2000mLKMnO4溶液 |
| B.用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸 |
| C.蒸馏时蒸馏烧瓶中液体的体积不能超过容积的2/3,液体也不能蒸干 |
| D.将金属钠在研体中研成粉末,使钠与水反应的实验更安全 |
从下列事实所列出的相应结论正确的是()
| 实验事实 |
结论 |
|
| A |
Cl2的水溶液可以导电 |
Cl2是电解质 |
| B |
SO2通入硝酸钡溶液出现白色沉淀 |
BaSO3不溶于强酸xx§kCom] |
C |
NaHCO3溶液与NaAlO2溶液混合产生白色沉淀 |
结合H+的能力:CO32-< AlO2- AlO2- |
| D |
常温下白磷可自燃而氮气须在放电时才与氧气反应 |
非金属性:P>N |