室温下,pH=13的NaOH溶液与pH=2的H2SO4溶液混合,所得混合溶液pH=12,则NaOH溶液与H2SO4溶液的体积比为
| A.11:2 | B.9:2 | C.2:11 | D.2:9 |
下列工业生产的主要化学反应,不牵涉勒沙特列原理的是
| A.合成氨工业 | B.硫酸工业 | C.氯碱工业 | D.纯碱工业 |
下列金属冶炼的反应原理错误的是
A.2AlCl3(熔融) 2Al + 3Cl2↑ 2Al + 3Cl2↑ |
B.CuO + H2 Cu + H2O Cu + H2O |
C.Fe3O4 + 4CO 3Fe +4CO2 3Fe +4CO2 |
D.2HgO 2Hg + O2↑ 2Hg + O2↑ |
下列关于晶体的叙述错误的是
| A.分子晶体中可能不含共价键 | B.原子晶体中只存在共价键 |
| C.离子晶体中一定含有离子键 | D.分子晶体中可能含有离子键 |
随着科学技术的不断进步,研究物质的手段和途径越来越多,N5+、H3、O4、C60等已被发现。下列有关说法中,正确的是
| A.N5+离子中含有36个电子 | B.O2与O4属于同位素 |
| C.C60是原子晶体 | D.H2与H3属于同素异形体 |
下列表示式正确的是
A.甲烷的球棍模型: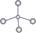 |
B.CO2分子的比例模型: |
| C.淀粉分子的最简式:CH2O | D.乙烯的结构简式 CH2 = CH2 |