在2 L的密闭容器中进行如下反应:CO(g)+H2O(g)
 CO2(g)+H2(g),有如下数据:
CO2(g)+H2(g),有如下数据:
| 实验 |
温度/℃ |
起始量/mol |
平衡量/mol |
|||
| CO |
H2O |
CO2 |
H2 |
CO2 |
||
| 1 |
650 |
2.0 |
1.0 |
0 |
0 |
0.8 |
| 2 |
800 |
2.0 |
2.0 |
0 |
0 |
1.0 |
下列说法正确的是
A.正反应为放热反应
B.实验1中,CO的转化率为80%
C.650℃时,化学平衡常数K=
D.实验1再加入1.0 mol H2O,重新达到平衡时,n(CO2)为1.6 mol
下列微粒中,对水的电离平衡不产生影响的是()
A.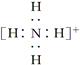 |
B.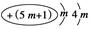 |
C.26R3+ | D. |
下列说法中正确的是()
| A.6.8 g熔融KHSO4与3.9 g熔融Na2O2中阴离子数目相同 |
B.某金属阳离子的结构示意图为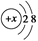 ,其与Cl-形成的强电解质都是离子化合物 ,其与Cl-形成的强电解质都是离子化合物 |
C.二硫化碳是直线形非极性分子,其电子式为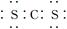 |
| D.中子数为18的氯原子可表示为18Cl |
下列化学用语的使用正确的是()
| A.K+与Ar的结构示意图相同 |
B.Na2O的电子式是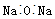 |
| C.通常状况下,1.5 mol氧气与0.5 mol氮气混合后气体的总体积为44.8 L |
D.乙烷、乙烯和苯的结构简式分别为CH3CH3、CH2=CH2和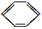 |
“纳米材料”是粒子直径为几纳米至几十纳米的材料,纳米碳就是其中一种。若将纳米碳均匀地分散到蒸馏水中,所形成的物质()
①是溶液;②是胶体;③能产生丁达尔效应;④能透过滤纸;⑤不能透过滤纸;⑥静置后会析出黑色沉淀
| A.①④⑤ | B.②③④ |
| C.②③⑤ | D.①③④⑥ |
下列有关物质的性质与应用相对应的是()
| A.NH3极易溶于水,可用作制冷剂 |
| B.Al2O3熔点高,可用作耐高温材料 |
| C.SO2具有氧化性,可用于漂白品红、织物等 |
| D.BaCO3能与盐酸反应,可用于治疗胃酸过多 |