同学在帮助老师整理实验室时,发现了半瓶久置的氢氧化钙粉末,他们决定对这瓶氢氧化钙粉末的组成进行实验探究.
(1)提出问题:这瓶氢氧化钙是否已经变质?
(2)猜想与假设:该氢氧化钙粉末的成分为
I.氢氧化钙;
II.氢氧化钙、碳酸钙;
III._____①_________.
(3)设计方案、进行实验:请你参与探究,并填写下表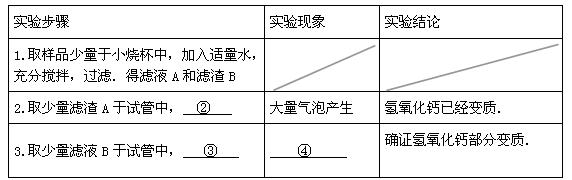
(4)联想与启示:氢氧化钙变质的原因___________⑤_________(用化学方程式表示),因此氢氧化钙应___⑥_____保存.
(5)【定量分析】为了进一步探究该氢氧化钙样品中各成分的质量,小组同学称取氢氧化钙样品12.4g于锥形瓶中,加入32.6g水,振荡形成悬浊液,向锥形瓶中逐滴滴加的稀盐酸,使其充分反应至无气体产生,测得加入盐酸的质量与锥形瓶中物质的质量关系如下表所示。
| 加入盐酸的质量/g |
0 |
25 |
37.5 |
| 锥形瓶中物质的质量/g |
45 |
70 |
80.3 |
(I)根据表中数据分析,加入盐酸的质量在0到25克时,仅有_⑦___与盐酸反应
(II)试求12.4g该样品中各成分的质量.
将20g含杂质(杂质不溶于水,也不溶于酸)的锌样品,与一定质量的稀硫酸恰好完全反应,所得溶液质量80.5g,同时生成氢气0.4g,试计算:
(1)样品中锌的质量为:g。
(2)完全反应后所得溶液中溶质的质量分数(写出计算过程)。
型禽流感是一种新型禽流感,于2013年3月底在上海和安徽两地率先发现,已经造成多人死亡,帕拉米韦是一种新型的抗流感病毒药物,属神经氨酸酶抑制剂,对抑制 禽流感有一定的效果,其化学式为: (其相对分子质量为328),回答以下问题:
(1)帕拉米韦是由种元素组成.
(2)帕拉米韦中H、N两种元素的质量比为:;
(3)帕拉米韦中碳元素的质量分数为:.
小亮同学对在空气中放置一段时间的"铜树"(铝丝浸泡在硫酸铜溶液制成如右图)的的成分时行分析,取出64.1克固体样品,用10%的盐酸充分溶解,溶液呈无色,产生的气体和剩余固体随消耗10%的盐酸质量变化关系曲线如下图:
结合图中数据分析:
(1)读图可知,
元素的质量
,
"铜树"有
、(填化学式)
(2)请结合化学方程式计算该"铜树"中
元素的质量分数?
(3)只知道"铜树"质量
和消耗10%的盐酸总质量(
),也能求出"铜树"中铝元素质量分数,其表达式为(用
表示,可不化简)
某实验需要
的
(1)该溶液的溶质质量是
,从中取
溶液,此溶液的质量分数为。
(2)实验室用硫酸铜晶体(分子式为
)配制
克
的硫酸铜溶液,需称取硫酸铜晶体
。(已知相对分子质量:
为
,
为
)
钠与水反应生成NaOH和H2(2Na+2H2O=2NaOH+H2↑),现向95.6克水中加入4.6克钠,充分反应(有水剩余)。
求:(1)生成NaOH的质量是多少?
(2)反应后溶液中溶质的质量分数是多少?