关于苯的叙述中错误的是
| A.苯在催化剂作用下能与液溴发生取代反应 |
| B.在苯中加入酸性KMnO4溶液,振荡并静置后下层液体为紫色 |
| C.在苯中加入溴水,振荡并静置后下层液体为橙黄色 |
| D.在一定条件下,苯能与氯气发生加成反应 |
已知M、W、X、Y、Z是短周期中原子序数依次增大的5种主族元素,其中W、Z同族,M原子的最外层电子数是电子层数的3倍,元素X在同周期的主族元素中原子半径最大,Y是地壳中含量最多的金属元素。下列说法中正确的是
| A.气态氢化物稳定性最强的是HZ |
| B.Y的单质可通过电解熔融的Y与Z形成的化合物获得 |
| C.原子半径由小到大的顺序为rW<rM<rY |
| D.X的焰色反应通过蓝色的钴玻璃呈紫色 |
氮化硅(Si3N4)是一种具有耐高温等优异性能的新型陶瓷,工业上可用下列方法制取:
工业上可用下列方法制取:3SiO2+6C+2N2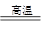 Si3N4+6CO.下列说法正确的是
Si3N4+6CO.下列说法正确的是
| A.氮化硅晶体属于分子晶体 |
| B.氮化硅中氮元素的化合价为-3 |
| C.上述反应中,N2是还原剂,SiO2是氧化剂 |
| D.上述反应中,每生成1mol Si3N4,N2得到6mol电子 |
下列说法正确的是
| A.分子式为H2O和D2O的性质相同 |
| B.相同条件下,等质量的碳按a、b两种途径完全转化,途径a和途径b放出的热能相等 途径a:C  CO+H2 CO+H2 CO2+H2O CO2+H2O途径b:C  CO2 CO2 |
| C.PM2.5是指大气中直径接近2.5×10-6m的颗粒物,分散在空气中形成胶体 |
| D.氢氧燃料电池的能量转换形式仅为化学能转化为电能 |
下列有关硫元素及其化合物的表示正确的是
| A.质量数为34、中子数为18的核素:3416S |
B.S2-的结构示意图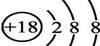 |
| C.CS2的结构式:S—C—S |
D.亚硫酸的电离方程式:H2SO3 2H++SO32- 2H++SO32- |
化学与科学、技术、社会、环境密切相关,下列说法错误的是
| A.神舟九号升空时火箭发射的动力主要来源于化学能 |
| B.洁厕灵的主要成分是盐酸,不能与“84”消毒液混用 |
| C.采用催化转换技术将汽车尾气中的NOx和CO转化为无毒气体 |
| D.为了能增加水中氧气的含量,养金鱼用的自来水一般先在阳光下晒一段时间 |