下列叙述正确的是
| A.等物质的量的硫蒸气和硫粉分别完全燃烧,后者放出热量多 |
| B.稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,若将含0.5 mol H2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ |
| C.C(石墨,s)=C(金刚石,s) ΔH=+1.9 kJ·mol-1,则说明金刚石比石墨稳定 |
D.反应2CO(g)+2NO(g) N2(g)+2CO2(g)在298 K时能自发进行,则它的,ΔS>0 N2(g)+2CO2(g)在298 K时能自发进行,则它的,ΔS>0 |
青石棉(crocidolite)是一种致癌物质,是《鹿特丹公约》中受限制的46种化学品之一,其化学式为Na2Fe5Si8O22(OH)2。青石棉用稀硝酸溶液处理时,还原产物只有NO,下列说法不正确的是
| A.青石棉是一种硅酸盐产品 |
| B.青石棉中含有一定量的石英晶体 |
| C.青石棉的化学组成可表示为Na2O·3FeO·Fe2O3·8SiO2·H2O |
| D.1 mol青石棉能使1 mol HNO3被还原 |
分类法是学习化学的重要方法,人们在认识事物时可采用多种分类方法。下列(2)中的物质不能与(1)中的物质归为一类的是
| 选项 |
(1) |
(2) |
| A |
FeSO4、NO2、MnO2、NaClO、Cu3P、Na2O2 |
H2SO3 |
| B |
CH3COOH、HOOC—COOH、HClO、H2S |
HF |
| C |
复分解反应、电解反应、放热反应、离子反应 |
焰色反应 |
| D |
(NH4)2SO4、NH4Cl、NH4NO3、NH3·H2O |
NH4HCO3 |
为了检验某固体物质中是否含有NH4+,下列试纸和试剂一定用不到的是
①蒸馏水 ②NaOH溶液 ③红色石蕊试纸 ④蓝色石蕊试纸 ⑤稀硫酸
| A.①⑤ | B.④⑤ | C.①③ | D.①④⑤ |
下列各项中,表达正确的是
| A.甲醛的结构简式:HCOH | B.C2H2分子的结构式:CH≡CH |
C.CH4分子的比例模型: |
D.异丁烷的键线式: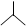 |
在杠杆的两端分别挂着质量和体积都相同的铝球和铁球,此时杠杆平衡。然后将两球分别浸没在氢氧化钠溶液和硫酸铜溶液中片刻(如下图所示),则下列说法正确的是
| A.两烧杯中均无气泡产生 | B.左边烧杯中的溶液质量减少了 |
| C.去掉两烧杯,杠杆仍平衡 | D.右边铁球上出现红色 |