(12分)稀土元素是周期表中ⅢB族钪、钇和镧系元素之总称,金属活泼性仅次于碱金属和碱土金属元素,它们的性质极为相似,常见化合价为+3价。无论是航天、航空、军事等高科技领域,还是传统工农业,稀土的应用几乎是无所不在。其中钇(Y)元素是激光和超导的重要材料。我国蕴藏着丰富的含钇矿石(Y2FeBe2Si2O10),工业上通过如下生产流程可获得氧化钇。
已知:
①有关金属离子形成氢氧化物沉淀时的pH见下表。
| 离子 |
开始沉淀时 的pH |
完全沉淀时 的pH |
| Fe3+ |
2.7 |
3.7 |
| Y3+ |
6.0 |
8.2 |
②Be(OH)2+2NaOH Na2BeO2+2H2O
Na2BeO2+2H2O
请回答下列问题:
(1)过滤Ⅲ所得滤液的溶质主要有______________。
(2)①欲从过滤I所得混合溶液中制得Be(OH)2沉淀,最好选用盐酸和________两种试剂,再通过必要的操作即可实现。
a.NaOH溶液 b.氨水 c.CO2 d.HNO3
②写出Na2BeO2与足量盐酸发生反应的离子方程式 。
(3)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,则该温度下反应Fe3++3H2O Fe(OH)3+3H+的平衡常数K= 。
Fe(OH)3+3H+的平衡常数K= 。
(4)写出煅烧过程的化学方程式 。
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A.0.1 mol·L-1 NaOH溶液:K+、Ba2+、Cl-、HCO3- |
| B.0.1 mol·L-1 Na2CO3溶液:K+、NH4+、NO3-、SO42- |
| C.0.1 mol·L-1 FeCl3溶液:K+、Na+、I-、SCN- |
| D.0.1 mol·L-1 HCl的溶液:Ca2+、Na+、ClO-、NO3- |
用试纸检验气体性质是一种重要的实验方法。如图所示的实验中(可加热),下列试纸的选用、现象、对应结论都正确的一项是( )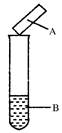
| 选项 |
试剂B |
湿润的试纸A |
现象 |
结论 |
| A |
碘水 |
淀粉试纸 |
变蓝 |
碘具有氧化性 |
| B |
浓氨水,生石灰 |
蓝色石蕊试纸 |
变红 |
氨气为碱性气体 |
| C |
Na2SO3,硫酸 |
品红试纸 |
褪色 |
SO2具有漂白性 |
| D |
Cu,浓硝酸 |
KI淀粉试纸 |
变蓝 |
NO2为酸性气体 |
设nA为阿伏加德罗常数的值。下列说法正确的是( )
| A.1L1mol·L-1的NaClO 溶液中含有ClO-的数目为nA |
| B.1mol的羟基与1 mol的氢氧根离子所含电子数均为9nA |
| C.标准状况下,22.4L盐酸含有nA个HCl分子 |
| D.标准状况下,6.72L NO2与水充分反应转移的电子数目为0.2nA |
化学与社会、生产、生活紧切相关。下列说法正确的是( )
| A.煤经过气化和液化等物理变化可以转化为清洁燃料 |
| B.用聚氯乙烯代替聚乙烯作食品包装袋,有利于节约成本 |
| C.合成纤维、人造纤维及碳纤维都属于有机高分子材料 |
| D.“地沟油”禁止食用,但可以用来制肥皂 |
已知FeS2与某浓度的HNO3反应时生成Fe(NO3) 3、H2SO4和某单一的还原产物,若FeS2和参与反应的HNO3的物质的量之比为1:8,则该反应的还原产物是
| A.NO2 | B.NO | C.N2O | D.NH4NO3 |