X.Y、Z、W是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,己是由Z元素形成的单质。已知:甲+乙→丁+己,甲+丙→戊+己;0.1mol·L-1丁溶液的pH为13(25℃)。下列说法正确的是
| A.1mol甲与足量的乙完全反应共转移2mol电子 |
| B.Y元素在周期表中的位置为第3周期ⅣA族 |
| C.原子半径:W>Y>Z>X |
| D.1.0L0.1mol·L-1戊溶液中阴离子总的物质的量小于0.1mol |
下列各组离子可能大量共存的是
| A.能使碘化钾淀粉试纸变蓝的溶液:Na+、NH、S2-、Br- |
| B.遇pH试纸变红色的溶液:Fe2+、S2O、SO42-、Na+ |
| C.水电离出的c(H+) •c(OH-) =10-28的溶液:Na+、S2-、NO3-、SO32- |
| D.能使KSCN显红色的溶液:Na+、NH4+、AlO、CO |
相对分子质量为128的有机物A完全燃烧只生成CO2和H2O,若A含一个六碳环且可与NaHCO3溶液反应,则其环上一溴代物的数目为
| A.1 | B.2 | C.3 | D.4 |
某课外实验小组设计的下列实验不合理的是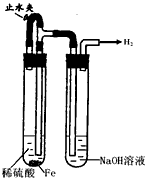
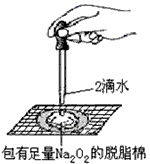
A装置①制备并观察氢氧化亚铁 B.装置②证明过氧化钠与水反应放热

C.装置③比较KMnO4、Cl2、 D.装置④测定盐酸的浓度
I2的氧化性强弱
气体的自动化检测中常常应用原电池原理的传感器。下图为电池的工作示意图:气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号。下表列出了待测气体及敏感电极上部分反应产物。则下列说法中正确的是
| 待测气体 |
部分电极反应产物 |
| NO2 |
NO |
| Cl2 |
HCl |
| CO |
CO2 |
| H2S |
H2SO4 |
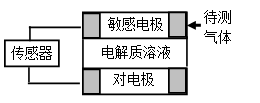
A.上述气体检测时,敏感电极均作电池正极
B.检测Cl2气体时,敏感电极的电极反应为:Cl2 + 2e-= 2Cl-
C.检测H2S气体时,对电极充入空气,对电极上的电极反应式为O2 + 2H2O+ 4e- = 4OH-
D.检测H2S和CO体积分数相同的两份空气样本时,传感器上产生的电流大小相同
下列说法不正确的是
A.已知H2(g)+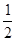 O2(g)===H2O(g) ΔH1=a kJ·mol-1; O2(g)===H2O(g) ΔH1=a kJ·mol-1;2H2(g)+O2(g)===2H2O(g) ΔH2=b kJ·mol-1,则a>b |
| B.CO的燃烧热为283.0 kJ·mol-1,则 2CO2(g)===2CO(g)+O2(g) ΔH=+566.0 kJ·mol-1 |
C.若N2(g)+3H2(g)  2NH3(g) ΔH=-d kJ·mol-1,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出的热量小于d kJ 2NH3(g) ΔH=-d kJ·mol-1,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出的热量小于d kJ |
| D.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和KOH反应的中和热ΔH=-114.6 kJ·mol-1 |