K, Fe, C, N, O, S是中学化学常见的六种元素。
(1)K位于元素周期表的第 周期第 族;N的基态原子核外有 个未成对电子。基态Fe2+的核外电子排布式是
(2)用“>”或“<”填空: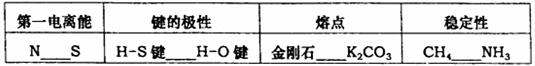
(3)在250C、l01kPa下,已知CO与NO在一定条件下反应生成N2和CO2,恢复至原状态,平均每转移lmol电子放热153.9kJ,该反应的热化学方程式是
(4)钢铁在有电解质溶液存在的条件下易发生电化学腐蚀。某同学利用钢铁的电化学腐蚀原理,设计如图甲所示实验: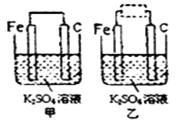
①写出石墨电极的电极反应式:
②将该装置作筒单修改即可成为铁的电化学防护装置,请在图乙中的虚线框内所示位置作出修改。
有铜片、锌片、若干小烧杯、导线、、盐桥(含琼胶的KCl饱和溶液)、电流计、ZnSO4溶液、CuSO4溶液,试画出原电池的装置图,并说明其工作原理。
⑴原电池装置图;⑵工作原理;
有A、B、C、D、E、Q六种元素,它们的核电荷数依次增大,A是元素周期表中原子半径最小的一种元素,B、C、D、E均比A多一个电子层,且B、C、D、E是连继相邻的四种元素,其中E是元素周期表中非金属性最强的一种元素,Q的核电荷数是A、B、D、E的核电荷数的总和,按要求完成下列问题:
⑴.这几种元素中电负性最大的是()(填元素符号,下同);
⑵.B、C、D、E的第一电离能由小到大的顺序是(),原子半径由大到小的顺序是();
⑶.C的氢化物的电子式是(),C的氢化物结构式是(),C的最高价氧化物对应的水化物的化学式是(),C的最高价氧化物对应的水化物和C的最低价氢物形成的化合物的化学式是();
⑷.Q的电子排布式是(),Q的价电子排布式是(),Q的价电子排布图是()。
⑸.说出D、Q在周期表中的分区,D在()区,Q在()区, D原子核外有()个成单电子.
⑹.元素B在周期表中位于第()周期,第()族。
在一定温度下,向一2L固定容积的密闭容器中通入20 molN2和60 molH2,经过5分钟后,N2的浓度是5mol∕L,又过了5分钟 N2、H2、NH3的浓度不再变化,此时NH3的浓度是14 mol∕L,达到平衡后共放出QKJ的热量,试完成下列问题:
⑴前5分钟用H2表示的化学反应速率();
⑵反应达到平衡后N2的转化率();
⑶表示该温度下合成氨的化学平衡常数的表达式为();
⑷若平衡后再增大压强,化学平衡向()方向移动(填“正”“逆”“不”);
⑸该温度下反应的热化学方和式为()(用含Q的式子表示);
⑹在该温度下,向另一2L固定容积的密闭容器中通入N2 5 mol、H215 mol、NH330 mol,反应达到平衡后H2的浓度是()。
按要求完成下列问题。
⑴.写出铅蓄电池放电时的总反应和两个电极反应及反应类型
放电总反应:
负极:()反应;
正极:()反应;
⑵.写出氯碱工业中电解饱和食盐水的总反应和两个电极反应及反应类型
电解总反应:
阳极:()反应;
阴极:()反应;
⑶.氢氧燃料电池中用KOH做电解质溶液,H2是还原剂,O2是助燃剂,写出正、负两极的电极反应
负极:正极:
下图转化关系中A—H为中学化学常见化合物,甲、乙、丙、丁为常见单质,其中甲、丁常温为气体。已知单质乙、化合物A为黄色(或淡黄色)固体。乙经过连续与甲反应后,再与水化合,是工业上制H的反应过程。B、F两种气体都能使澄清石灰水变浑浊。(部分反应物或产物略去)
(1)写出下列物质的化学式:A________ F________ 甲_______ 丙________ .
(2)按要求完成下列反应:
A与B反应的化学方程式 ____________________________________;
丙与D溶液反应的离子方程式_________________________________。
(3)鉴别B和F的方法_____________________________________________。