碱性硼化钒(VB2)—空气电池工作时反应为:4VB2 + 11O2 = 4B2O3 + 2V2O5。用该电池为电源,选用惰性电极电解硫酸铜溶液,实验装置如图所示。当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是
| A.VB2电极发生的电极反应为:2VB2 + 11H2O - 22e- = V2O5 + 2B2O3 + 22H+ |
| B.外电路中电子由c电极流向VB2电极 |
| C.电解过程中,b电极表面先有红色物质析出,然后有气泡产生 |
| D.若B装置内的液体体积为200 mL,则CuSO4溶液的物质的量浓度为0.05 mol/L |
下列操作方法或仪器选择正确的是()
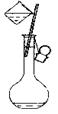 20℃ 250mL |
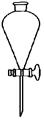 |
 |
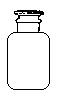 |
| A.配置一定物质的量浓度的溶液 |
B.分离水和乙醇 |
C.收集氨气 |
D.用带玻璃塞的试剂瓶盛放NaOH溶液 |
131 53I是一种人工放射性核素,下列关于131 53I的说法正确的是()
| A.质子数为78 | B.中子数为53 |
| C.与127 53I互为同位素 | D.核外电子数为131 |
石墨烯是由单层碳原子构成的新型材料(结构如图所示),可作为太阳能的电极。下列关于石墨烯的分类正确的是()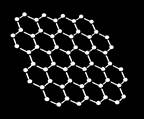
| A.属于共价化合物 | B.属于单质 | C.属于有机物 | D.属于电解质 |
联合国决定2011年为国际化学年,旨在纪念化学学科取得的成就及对人类的巨大贡献。下列科学家取得的成就与化学学科研究领域无关的是()
| A.哈伯发明合成氨技术 | B.门捷列夫发现元素周期律 |
| C.爱英斯坦提出相对论 | D.居里夫人发现镭 |
为了检验FeCl2溶液是否氧化变质,可向溶液中加入的试剂是()
| A.盐酸 | B.KSCN溶液 | C.氯水 | D.石蕊溶液 |