在25°C时,向10mL0.0lmol·L-1NaCN溶液中逐滴加人0.0lmol·L-1的盐酸,滴定曲线如图1所示,CN—、HCN浓度所占分数(α)随pH变化的关系如图2所示,下列表述正确的是 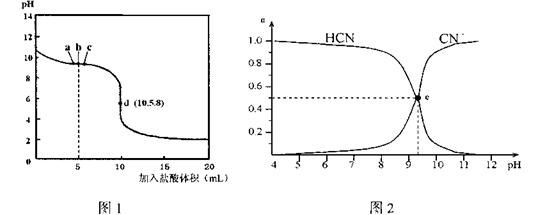
| A.b点时,溶液中微粒浓度大小的关系:c(CN-)>c(Cl-)>c(HCN)>c<(OH-)>c(H+) |
| B.d点溶液存在的关系:c(Na+)+c(H+)=c(HCN)+c(OH-)+2c(CN-) |
| C.图2中的e点对应图1中的c点 |
| D.在滴定过程中选用酚酞试剂比选用甲基橙试剂作指示剂误差更小 |
下列反应的离子方程式正确的是()
| A.将氢碘酸加到Fe(OH)3胶体中:Fe (OH)3 +3H+=Fe3++3H2O |
| B.碳酸氢钙溶液中加入少量烧碱:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+H2O |
| C.新制氯水中滴入少量溴化亚铁溶液:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
| D.锌与1mol«L-1HNO3溶液反应:Zn+2H+= Zn2++H2↑ |
对于敞口容器中的化学反应Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g) ,下列叙述 不正确的是
不正确的是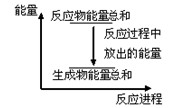

X、Y元素均为主族元素,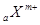 和
和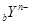 的电子层结构相同,则下列说法中不正确的是
的电子层结构相同,则下列说法中不正确的是
A.Y元素的核电荷数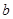 等于 等于 |
| B.Y的原子序数小于X的原子序数 |
C.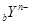 的离子半径小于 的离子半径小于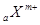 的离子半径 的离子半径 |
D.若X元素位于 周期,则Y元素位于 周期,则Y元素位于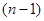 周期 周期 |
在化学学习与研究中类推的思维方法有时会产生错误的结论,因此类推的结论最终要经过实践的检验才能确定其正确与否。下列几种类推结论中,正确的是()
| A.SO2能与碱反应,推测:非金属氧化物都能与碱反应 |
| B.金属钠着火不能用CO2扑灭,推测:金属钾着火也不能用CO2扑灭 |
| C.Fe3O4可表示为FeO·Fe2O3,推测:Pb3O4也可表示为PbO·Pb2O3 |
| D.F-Cl-Br-I的单质熔点依次升高,推测:N-P-As-Sb-Bi的单质熔点也依次升高 |
在福岛核泄漏事故中,检测到的放射性物质包括碘—131、铯—137和钚—239等。硼具有阻止反应堆内核分裂,降低反应堆温度的功能。下列说法正确的是()
| A.钚—239的质子数为239 | B.氢氧化铯的碱性比氢氧化钾强 |
| C.碘元素的相对原子质量为131 | D.硼酸的酸性比铝酸(氢氧化铝)弱 |